
| A. | ①④⑥ | B. | ②③⑤⑥ | C. | ②⑤⑥ | D. | ③⑤⑥ |
分析 ①CH3-CH=CH2和CH2=CH2的实验式都为CH2;
②煤的气化和液化为化学变化;
③C4H10和C6H14都为烷烃;
④同分异构体中,支链越多,则沸点越低;
⑤加入氢氧化钠溶液后,在滴加硝酸银溶液之前应加入硝酸酸化;
⑥测定相对分子质量的物理方法质谱法.
解答 解:①CH3-CH=CH2和CH2=CH2都为烯烃,实验式都为CH2,故正确;
②煤的气化生成CO、氢气等,液化生成甲醇等,为化学变化,故错误;
③C4H10和C6H14都为烷烃,二者互为同系物,故正确;
④同分异构体中,支链越多,则沸点越低,则正戊烷、异戊烷、新戊烷的沸点逐渐变低,故正确;
⑤在碱性条件下水解生成溴化钠,检验溴离子,应加入硝酸酸化,以避免生成AgOH等沉淀而干扰实验现象,故错误;
⑥测定相对分子质量的物理方法质谱法,故错误.
故选C.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,有利于培养学生良好的科学素养,注意把握有机物的结构和官能团的性质,注意同系物以及同分异构体的判断,难度不大.


科目:高中化学 来源: 题型:选择题

| A. | 装置甲中铜片表面产生气泡 | |
| B. | 装置甲中正极的电极反应式:2H++2eˉ=H2↑ | |
| C. | 装置乙中电流从铜片经导线流向锌片 | |
| D. | 装置乙溶液中SO42ˉ向铜片做定向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
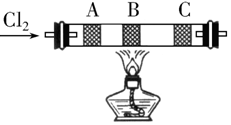 在硬质玻璃管中的A、B、C处依次放有浸有KBr溶液、KI溶液、淀粉(已知淀粉遇I2显蓝色)溶液的3个棉球(如图所示).由左端通入氯气,在B处加热,可观察到A处棉球呈橙色,B处棉球呈现黄色,C处棉球呈蓝色.将玻璃管冷却后,在B、C之间的玻璃壁上有紫黑色的固体(填物质状态),这是因为碘易升华.A、B两处发生的离子方程式分别是:Cl2+2Br-=Br2+2Cl-、Cl2+2I-=I2+2Cl-.
在硬质玻璃管中的A、B、C处依次放有浸有KBr溶液、KI溶液、淀粉(已知淀粉遇I2显蓝色)溶液的3个棉球(如图所示).由左端通入氯气,在B处加热,可观察到A处棉球呈橙色,B处棉球呈现黄色,C处棉球呈蓝色.将玻璃管冷却后,在B、C之间的玻璃壁上有紫黑色的固体(填物质状态),这是因为碘易升华.A、B两处发生的离子方程式分别是:Cl2+2Br-=Br2+2Cl-、Cl2+2I-=I2+2Cl-.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气能溶于水 | |
| B. | 氯气是一种有毒气体 | |
| C. | 氯气是一种黄绿色、有刺激性气味的气 | |
| D. | 氯气、液氯和氯水是同一种物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烷中混有乙烯可用酸性高锰酸钾溶液来除去 | |
| B. | 在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 | |
| C. | 已知2SO2(g)+O2(g)?2SO3(g)△H<0,该反应在任何温度下均可自发进行 | |
| D. | 室温下,Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=9.0×10-12,向浓度相等的Na2CrO4和NaCl的混合稀溶液中滴加0.01 mol•L-1 AgNO3溶液,先生成Ag2CrO4沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 物质 | 熔点 | 沸点 | 水反应性 |
| SiCl4 | -70℃ | 57.6℃ | 强烈水解 |
| CCl4 | -22.9℃ | 76.8℃ | 稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 锌银(Zn-Ag2O)电池多应用于军事、航空、移动的通信设备、电子仪器和人造卫星、宇宙航行等方面,用如图所示装置模拟其工作原理,下列说法正确的是( )
锌银(Zn-Ag2O)电池多应用于军事、航空、移动的通信设备、电子仪器和人造卫星、宇宙航行等方面,用如图所示装置模拟其工作原理,下列说法正确的是( )| A. | K+向a极移动 | |
| B. | b 极的电极反应式为 Ag2O+H2O+2e-═2Ag+2OH- | |
| C. | 用该电池给铁棒镀铜,则铁棒与 b 极相连 | |
| D. | 电池工作一段时间后,电解液的pH减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol MnO2 与 40 mL 10 mol/L 的浓盐酸充分反应,生成的氯气分子数为 0.1NA | |
| B. | lmol FeI2与足量氯气反应时转移的电子数为2NA | |
| C. | 分子数目为 0.1NA的 N2 和 NH3 混合气体,原子间含有的共用电子对数目为 0.3NA | |
| D. | 用惰性电极电解 CuSO4 溶液一段时间后,若加入 0.05mol 的 Cu2(OH)2CO3 固体恰好能使溶液恢复到原来的浓度,则该电解过程中转移电子的数目为 0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com