在火箭推进器中装有还原剂肼(N
2H
4)和强氧化剂H
2O
2,当它们混合时,即产生大量的氮气和水蒸气,并放出大量的热。已知0.4mol液态肼和足量H
2O
2反应生成氮气和水蒸气时放出256.64kJ的热量。
(1)在结构上N
2H
4和NH
3的关系有如H
2O
2和H
2O的关系。N
2H
4能发生下列反应:
N
2H
4+H
3O
+=N
2H
5++H
2O
N
2H
4+H
2O
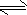
N
2H
5++OH
-
N
2H
5++H
2O
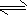
N
2H
62++OH
- N
2H
5++H
2O

N
2H
4+H
3O
+ 据此可得出的结论是______________。
A.肼水解显酸性
B.肼在水中可电离出H
+离子
C.肼是二元弱碱
D.肼是二元弱酸
(2)写出肼和H
2O
2反应的热化学方程式_______________________。
(3)已知H
2O(1)==H
2O(g) △H=+44kJ/mol,则16g液态肼与足量双氧水反应生成氮气和液态水时,放出的热量是___________________________。
(4)上述反应应用于火箭推进器,除释放出大量热量和快速产生大量气体外,还有一个很突出的优点是
_____________________。
(5)用氨和次氯酸钠按一定的物质的量之比混合可生成肼,写出反应的化学方程式__________________________,该反应的还原产物是___________________。

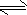 N2H5++OH-
N2H5++OH-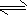 N2H62++OH-
N2H62++OH-  N2H4+H3O+
N2H4+H3O+  云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案