
【题目】属于天然高分子化合物的是( )
A.塑料B.纤维素C.葡萄糖D.乙酸
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:高中化学 来源: 题型:
【题目】乙酸乙酯是制药工业和有机合成中的重要原料,实验室制备乙酸乙酯的实验装置![]() 夹持及加热装置已略去
夹持及加热装置已略去![]() 、有关数据和实验步骤如下所示。
、有关数据和实验步骤如下所示。
物质 | 相对分子质量 | 密度 | 沸点 | 在水中的溶解性 |
乙醇 | 46 |
| 80 | 以任意比互溶 |
乙酸 | 60 |
| 118 | 易溶 |
乙酸乙酯 | 88 |
| 77 | 难溶 |
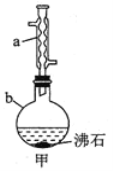
实验步骤:
![]() 向仪器b中加入9.5 mL乙醇(过量)和6 mL乙酸,再缓慢加入2.5 mL浓硫酸,混合均匀后,加入沸石,然后装上冷凝管
向仪器b中加入9.5 mL乙醇(过量)和6 mL乙酸,再缓慢加入2.5 mL浓硫酸,混合均匀后,加入沸石,然后装上冷凝管![]() 如图甲所示
如图甲所示![]() 。
。
![]() 小火加热仪器b,缓慢回流0.5 h,待瓶内反应物冷却后,将回流装置改成蒸馏装置,加热蒸出乙酸乙酯。
小火加热仪器b,缓慢回流0.5 h,待瓶内反应物冷却后,将回流装置改成蒸馏装置,加热蒸出乙酸乙酯。
![]() 向馏出液中缓慢加入5mL饱和碳酸钠溶液,振荡,直至不再有二氧化碳气体产生,然后将混合液转移至分液漏斗中,分去水层,将有机层依次用5mL饱和食盐水和5mL饱和氯化钙溶液洗涤后,转移至锥形瓶中,加入少量无水
向馏出液中缓慢加入5mL饱和碳酸钠溶液,振荡,直至不再有二氧化碳气体产生,然后将混合液转移至分液漏斗中,分去水层,将有机层依次用5mL饱和食盐水和5mL饱和氯化钙溶液洗涤后,转移至锥形瓶中,加入少量无水![]() 固体,静置片刻,过滤除去
固体,静置片刻,过滤除去![]() 固体,然后将有机层进行蒸馏纯化,收集
固体,然后将有机层进行蒸馏纯化,收集![]() 时的馏分,得到
时的馏分,得到![]() 乙酸乙酯。
乙酸乙酯。
请回答下列问题:
(1)实验原理:乙酸与乙醇在催化剂存在的条件下加热可以发生酯化反应生成乙酸乙酯,请用氧同位素示踪法写出CH3CO18OH与CH3CH2OH发生酯化反应的化学方程式。______________。
(2)仪器a的名称为______________,仪器b的规格为_______![]() 填字母
填字母![]() 。
。
A.25 mL B.50mL C.250 mL D.500mL ![]()
(3)步骤![]() 中,将馏出液经饱和碳酸钠溶液处理后的混合液置于分液漏斗中,振荡后静置,水层在________
中,将馏出液经饱和碳酸钠溶液处理后的混合液置于分液漏斗中,振荡后静置,水层在________![]() 填“上层”或“下层”
填“上层”或“下层”![]() 。
。
(4)在步骤![]() 中,加入少量无水硫酸镁固体的作用是__________________________。
中,加入少量无水硫酸镁固体的作用是__________________________。
(5)酯层厚度的标定:加热回流一段时间后再蒸出产物,为了更好地测定有机层厚度,可预先向饱和碳酸钠溶液中加入1滴_________试液,现象是 ___________________。
(6)该实验中乙酸乙酯的产率为_______ (计算结果精确到![]() )。
)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,A与B反应可生成C和D,其能量变化如图:

(1)下列有关反应A+B=C+D的说法正确的是________。
A.反应前后原子的种类和数目一定不变
B.该反应若有热量变化,则一定是氧化还原反应
C.若该反应为放热反应,则不需要加热反应就一定能自发进行
D.反应物的总质量、总能量与反应产物的总质量、总能量均相等
(2)若E1<E2,则反应产物的总能量________(填“>”“<”或“=”)反应物的总能量,反应热Q________0(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,把试管放入盛有25 ℃饱和Ca(OH)2溶液的烧杯中,试管开始放入几小块镁片,再用滴管滴5 mL盐酸于试管中。请回答下列问题:

(1)实验中观察到的现象是______________________________________________________。
(2)产生上述现象的原因是___________________________________。
(3)写出有关的离子方程式:________________________________________。
(4)由实验推知,MgCl2溶液和H2的总能量________(填“大于”“小于”或“等于,下同”)镁片和盐酸的总能量,ΔH________0。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法不正确的是( )
A. 0.1 mol![]() 所含电子的数目为1.4NA
所含电子的数目为1.4NA
B. 32gS8(分子结构:![]() )中的共价键数目为NA
)中的共价键数目为NA
C. 14gLi在空气中充分燃烧,消耗氧分子的数目为NA
D. 标准状况下,11.2LCl2溶于水,溶液中Clˉ、ClOˉ和HClO的微粒数之和小于NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可用软锰矿(主要成分是MnO2)和黄铁矿(主要成分是FeS2)为主要原料制备高性能磁性材料碳酸锰(MnCO3)。其工业流程如下:

回答下列问题:
(1)为了提高溶浸工序中原料的浸出率,除了可以搅拌、将矿石研磨粉碎以外,可以采取的措施有(写两条)________________。
(2)副产品A的化学式是________________。
(3)净化工序的目的是除去溶液中的Cu2+、Ca2+等杂质。若测得滤液中c(F-)=0.01 mol·L-1,则滤液中残留的c(Ca2+)=________________〔已知:Ksp(CaF2)=1.46×10-10〕。
(4)沉锰工序中,加入NH4HCO3后有无色无味的气体放出,同时有浅红色的沉淀生成,发生反应的离子方程式是________________;沉锰工序中判断沉淀已经洗涤干净的实验操作是________________。
(5)已知MnCO3难溶于水和乙醇,潮湿时易被空气氧化,100℃开始分解。工业上一般用少量C2H5OH洗涤的原因是________________。
(6)溶浸过程中发生的主要反应如下,请完成并配平该反应的离子方程式:_____________ FeS2+_____________ MnO2+_____________ =_____________ Fe3++_____________ Mn2++_____________ SO42-+_____________ ,___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有① SiO2② Na2CO3③ (NH4)2CO3④ Al(OH)3四种物质,其中既能与盐酸反应,又能与NaOH溶液反应的是( )
A. ① ② B. ② ④ C. ③ ④ D. ① ② ③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列物质分类中,前者包含后者的是( )
序号 | 前者 | 后者 | 序号 | 前者 | 后者 |
A | 电解质 | 化合物 | B | 金属氧化物 | 碱性氧化物 |
C | 分散系 | 混合物 | D | 单质 | 纯净物 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com