
能促进水的电离,并使溶液中c(H+)>c(OH-)的操作是
①将水加热煮沸 ②向水中投入一小块金属钠 ③向水中通CO2
④向水中加入明矾晶体 ⑤向水中加NaHCO3固体 ⑥向水中加NaHSO4固体
A.①②④⑤ B.①④⑤ C.③④⑤ D.④
D
【解析】
试题分析::①加热时促进水的电离,但是氢离子和氢氧根浓度依然相等,故①错误;②加入金属钠,和水电离出的氢离子反应生成强氧化钠和氢气,使水的电离向右移动,碱性增强,c(H+)<c(OH-)故②错误;③二氧化碳溶于水形成碳酸,溶液中的c(H+)>c(OH-),酸对水的电离起抑制作用,故③错误;④向水中加入明矾,铝离子水解对水的电离起促进作用,电离后的溶液显酸性,溶液中的c(H+)>c(OH-),故④正确;⑤向水中加入NaHCO3,碳酸氢钠中的碳酸氢根水解显碱性,使溶液中的c(H+)<c(OH-),故⑤错误;⑥向水中加NaHSO4固体形成硫酸氢钠水溶液,硫酸氢钠在水中完全电离出钠离子、氢离子、硫酸根离子,氢离子对水的电离起抑制作用,故⑥错误.故选D.
考点:水的电离


科目:高中化学 来源:2014-2015学年湖南长沙市高三上学期第二次月考化学试卷(解析版) 题型:实验题
(14分)为探究某铁碳合金与浓硫酸在加热条件下反应的部分产物并测定铁碳合金中铁元素的质量分数,某化学活动小组设计了下图所示的实验装置,并完成以下实验探究。

往圆底烧瓶中加入mg铁碳合金,并滴入过量浓硫酸,点燃酒精灯。
(1)装置B的作用是______________________________________。
(2)甲同学观察到装置C中有白色沉淀生成。他得出了使澄清石灰水变浑浊的气体是二氧化碳的结论。装置A中能产生二氧化碳的化学方程式为_______________。
(3)乙同学认为甲同学的结论是错误的,他认为为了确认二氧化碳的存在,需在装置B~C之间添加装置M,装置E、F中盛放的试剂分别是_____、__________。重新实验后观察到装置F中的现象是__________。
(4)有些同学认为合金中铁元素的质量分数可用KMnO4溶液来测定(5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O)。测定铁元素质量分数的实验步骤如下;
I.往烧瓶A中加入过量的还原剂铜粉使溶液中的Fe3+完全转化为Fe2+过滤,得到滤液B;
II.将滤液B稀释为250 mL;
III.取稀释液25.00 mL,用浓度为c mol·L-1的酸性KMnO4溶液滴定,三次滴定实验所需KMnO4溶液体积的平均值为VmL。
①步骤II中,将滤液B稀释为250 mL需要用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还必须要用到的是___________________。
②滴定过程中_______________(填“需要”或“不需要")加入指示剂。
③铁碳合金中铁元素的质最分数为_____________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南邵阳县石齐学校高二上第一次月考化学(理)试卷(解析版) 题型:选择题
反应2Z(g) X(g)+ Y(g),△H>0。达到平衡时,下列说法正确的是( )
X(g)+ Y(g),△H>0。达到平衡时,下列说法正确的是( )
A.加入催化剂,X的产率增大
B.升高温度,Y的转化率增大
C.当容器活塞可活动时,充入稀有气体,平衡不移动
D.充入Z气体时,Z的转化率增大
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省衡阳市高二上学期期中考试化学试卷(解析版) 题型:选择题
下图表示2A(g)+B(g) 2C(g) ΔH<0,这个反应的正确图像为
2C(g) ΔH<0,这个反应的正确图像为
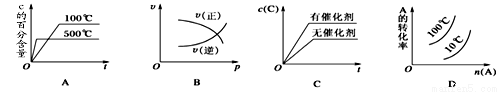
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省衡阳市高二上学期期中考试化学试卷(解析版) 题型:选择题
电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终点.如图是用KOH溶液分别滴定HCl溶液和CH3COOH溶液的滴定曲线示意图
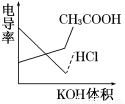
下列示意图中,能正确表示用NH3·H2O溶液滴定HCl和CH3COOH混合溶液的滴定曲线的是
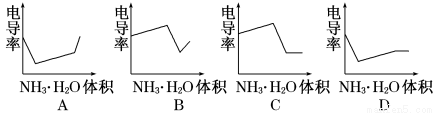
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省衡阳市高二上学期期中考试化学试卷(解析版) 题型:选择题
在C(s)+CO2(g)  2CO(g)反应中,可使反应速率增大的措施是
2CO(g)反应中,可使反应速率增大的措施是
①增大压强 ②增加碳的量 ③恒容下通入CO2
④恒压下充入N2 ⑤恒容下充入N2 ⑥恒容下通入CO
A.①③④ B.②④⑥ C.①③⑥ D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高三上学期第二次月考化学试卷(解析版) 题型:填空题
(8分)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产流程如下:
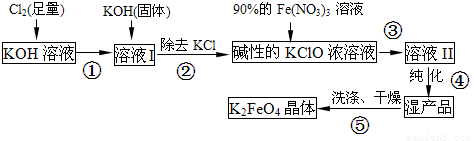
(1)配制KOH溶液时,是在每100 mL水中溶解61.6 g KOH固体(该溶液的密度为1.47 g/mL), 它的物质的量浓度是 ____mol/L。
(2)在溶液I中加入KOH固体的目的是 (填编号).
A.与溶液I中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使副产物KClO3转化为 KclO
(3)从溶液II中分离出K2FeO4后,还得到副产品KNO3、KCl,写出③中反应的离子方程式: 。
(4)高铁酸钾(K2FeO4)与水反应时,生成红褐色胶体的同时释放出一种具有氧化性的气
体单质,请写出该反应的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高三上学期第二次月考化学试卷(解析版) 题型:选择题
能正确表示下列反应的离子方程式的是( )
A.Cu溶于稀HNO3:Cu+2H++NO===Cu2++NO2↑+H2O
B.NaHCO3溶液中加入稀盐酸:CO+2H+===CO2↑+H2O
C.AlCl3溶液中加入过量稀氨水:Al3++4NH3·H2O===AlO+4NH+2H2O
D.向NaAlO2溶液中通入过量CO2制Al(OH)3: CO2+AlO+2H2O===Al(OH)3↓+HCO
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省浏阳市高一上第一次月考试卷化学试卷(解析版) 题型:填空题
(8分)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A、加热分解 B、结晶法 C、分液法 D、蒸馏法 E、过滤法
(1)___________分离饱和食盐水和沙子的混合物
(2)___________从硝酸钾和氯化钠的混合溶液中获得硝酸钾(溶解度差异很大)
(3)___________分离水和汽油的混合物
(4)___________分离四氯化碳(沸点为76.75°C)和甲苯(沸点为110.6°C)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com