
| 物质 | 熔点/℃ | 沸点/℃ | 其它性质 |
| SO2Cl2 | -54.1 | 69.1 | ①易水解产生大量白雾 ②易分解:SO2Cl2$\frac{\underline{\;△\;}}{\;}$SO2↑+Cl2↑ |
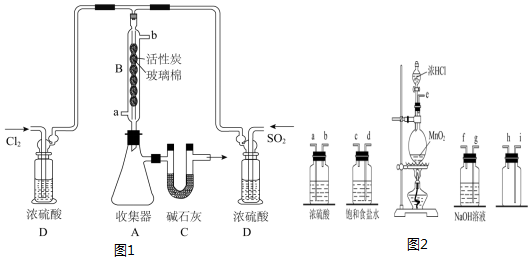
分析 I、(1)实验室由二氧化锰和浓盐酸共热制备氯气,制得的氯气混有水蒸气和HCl气体,用饱和食盐水吸收氯化氢气体,用浓硫酸吸收水蒸气,用排空气法收集氯气,最后用氢氧化钠吸收多余的氯气,防止污染空气;
II、(2)根据采用逆流的冷凝效果好,判断冷凝管的进水口;活性炭作催化剂;
(3)D装置的浓硫酸用来干燥气体,防止硫酰氯水解,同时还可以通过观察气泡控制气体流速;若无D,硫酰氯水解为硫酸和盐酸;
(4)硫酰氯受热易分解,可将收集器A放在冰水中冷却;
(5)C处U形管中碱石灰防止空气中的水蒸气进入装置,同时吸收挥发出去的二氧化硫和氯气,防止污染;
III、(6)①二者沸点相差较大,采取蒸馏法进行分离;
②氯磺酸(ClSO3H)分解:2ClSO3H═H2SO4+SO2Cl2,设计实验方案检验产品,需检验氢离子、检验硫酸根离子.
解答 解:I、(1)实验室由二氧化锰和浓盐酸共热制备氯气,制得的氯气混有水蒸气和HCl气体,用饱和食盐水吸收氯化氢气体,用浓硫酸吸收水蒸气,为充分吸收杂质气体,导气管长进短出,用排空气法收集氯气,氯气密度比空气大,导气管长进短出,最后用氢氧化钠吸收多余的氯气,防止污染空气;
故答案为:d;c;a;b;i;h;g;
II.(2)根据采用逆流的冷凝效果好,所以冷凝管中的冷却水进口为a,活性炭作催化剂;
故答案为:a;催化剂;
(3)D装置的浓硫酸用来干燥气体,防止硫酰氯水解,同时还可以通过观察气泡控制气体流速;若无D,硫酰氯水解为硫酸和盐酸.化学方程式为:SO2Cl2+2H2O═H2SO4+2HCl;
故答案为:通过观察气泡控制气体流速;SO2Cl2+2H2O═H2SO4+2HCl;
(4)硫酰氯受热易分解,可将收集器A放在冰水中冷却;
故答案为:合理,防止硫酰氯分解;
(5)二氧化硫、氯气为有毒的酸性气体,产物硫酰氯会水解,所以C处U形管中碱石灰可防止空气中的水蒸气进入装置,同时吸收挥发出去的二氧化硫和氯气;
故答案为:吸收多余二氧化硫、氯气,防止污染;防止水蒸气进入收集器使产品水解;
III、(6)①二者为互溶液体,沸点相差较大,采取蒸馏法进行分离;
故答案为:蒸馏;
②氯磺酸(ClSO3H)分解:2ClSO3H$\frac{\underline{催化剂}}{△}$H2SO4+SO2Cl2,取适量产品充分加热后加水稀释,分成两份,一份滴加紫色石蕊试液变红,另一份加入BaCl2溶液产生白色沉淀,说明含有H2SO4;
故答案为:取适量产品充分加热后加水稀释,分成两份,一份滴加紫色石蕊试液变红,另一份加入BaCl2溶液产生白色沉淀,说明含有H2SO4.
点评 本题考查物质的制备实验和实验设计,为侧重考查学生知识综合应用、根据实验目的及物质的性质进行排列顺、实验基本操作能力及实验方案设计能力,综合性较强,注意把握物质性质以及对题目信息的获取于使用,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 3:5 | C. | 2:3 | D. | 3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 我国目前最主要的能源是煤炭 | |
| B. | 人体运动所消耗的能量与化学反应无关 | |
| C. | 人类目前所直接利用的能量大部分是由化学反应所产生的 | |
| D. | 煤、石油、天然气是当今世界最重要的三种化石燃料 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一上10月月考化学试卷(解析版) 题型:实验题
某化学兴趣小组拟用下图装置测定某粗锌样品中锌的质量分数。他们查阅资料后获知该粗锌样品中的其他成分不能与稀盐酸反应。请填写以下实验报告。
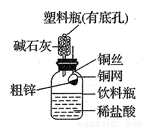
(1)实验目的: 。
(2)实验步骤:
①称取10.0g粗锌置于铜网中,按图示装置组装后,称得仪器和药品总质量为120.0g。
②将铜网插入足量的稀盐酸中,有关反应的化学方程式为 。
③反应完全后,称得装置总质量为119.8g,则粗锌中锌的质量分数为 。
(3)问题探究:(已知碱石灰是NaOH和CaO的混合物,常用于干燥、吸收气体)
①该实验若不用碱石灰,则所测得的粗锌中锌的质量分数将 (填“偏大”、“偏小”或“无影响”);
②若将粗锌换成某含有杂质的石灰石样品(杂质也不与稀盐酸反应),判断该实验方案能不能用于石灰石样品中CaCO3质量分数的测定,并说明理由____________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一上10月月考化学试卷(解析版) 题型:选择题
如图两瓶体积相等的气体在同温同压时瓶内气体关系一定正确的是( )
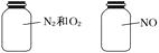
A.相同的质量 B.相同的摩尔质量
C.相同的密度 D.相同的原子数
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
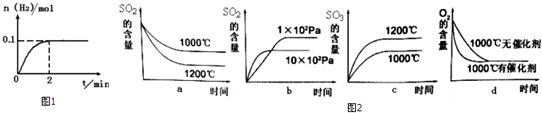
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2个甲基,可能生成4种一氯代物 | B. | 3个甲基,可能生成3种一氯代物 | ||
| C. | 3个甲基,可能生成5种一氯代物 | D. | 4个甲基,可能生成4种一氯代物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com