
| A、NaOH |
| B、HCl |
| C、Ba(OH)2 |
| D、H2SO4 |


 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
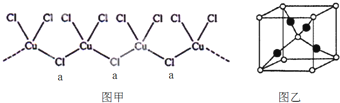
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使用无磷洗衣粉,可彻底解决水体富营养化问题 |
| B、应用高效洁净的能源转换技术有利于节能减排、保护环境 |
| C、用浸泡过高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可达到水果保鲜的目的 |
| D、合理开发利用可燃冰(固态甲烷水合物)有助于缓解能源紧缺 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲Pt 乙Pt 丙CuCl2 丁HCl气体 |
| B、甲C 乙Cu 丙CuSO4 丁CuO固体 |
| C、甲Pt 乙C 丙H2SO4 丁H2SO4(纯) |
| D、甲Fe 乙Fe 丙NaCl 丁NaOH固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、阳极发生氧化反应,其主要电极反应式:Ni2++2e-═Ni |
| B、电解过程中,阳极质量的减少与阴极质量的增加相等 |
| C、电解后,溶液中存在的金属阳离子有Fe2+,Zn2+和Ni2+ |
| D、电解后,电解槽底部的阳极泥中含有Cu,Pt和Fe |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com