
| A. | 常温下,pH=9的NaHA溶液:c(Na+)>c(HA-)>c(A2-)c(H2A) | |
| B. | Na2CO3溶液:c(H+)-c(OH-)=c(HCO3-)+2c(CO32-)-c(Na+) | |
| C. | 向NaOH溶液中滴入HCOOH溶液后溶液显碱性:c(HCOO-)>c(OH-)>c(H+) | |
| D. | 浓度均为0.1mol•L-1HF溶液与0.1mol•L-1KF溶液等体积混合:c(F-)+c(HF)=0.2mol•L-1 |
分析 A、常温下,pH=9的NaHA溶液说明溶液呈碱性,水解程度大于电离程度;
B、根据电荷守恒分析解答;
C、可能氢氧化钠过量,则c(OH-)>c(HCOO-)>c(H+);
D、根据物料守恒分析解答.
解答 解:A、常温下,pH=9的NaHA溶液说明溶液呈碱性,水解程度大于电离程度,所以离子浓度大小为:c(Na+)>c(HA-)>c(H2A)>c(A2-),故A错误;
B、根据电荷守恒,可知c(H+)+c(Na+)=c(OH-)+c(HCO3-)+2c(CO32-),所以c(H+)-c(OH-)=c(HCO3-)+2c(CO32-)-c(Na+),故B正确;
C、可能氢氧化钠过量,则c(OH-)>c(HCOO-)>c(H+),所以不一定符合,故C错误;
D、根据物料守恒,可知:c(F-)+c(HF)=$\frac{0.1×V+0.1×V}{2V}$=0.1mol•L-1,故D错误;
故选B.
点评 本题考查了离子浓度的大小,结合盐的水解,电荷的守恒和物料守恒综合分析题中信息,得出合理结论,本题难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 该化合物含有离子键和共价键 | |
| B. | 1molO2参与该反应时,得到1mol电子 | |
| C. | 该化合物中阳离子与阴离子个数比为2:1 | |
| D. | O2PtF6的熔点可能比O2低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 强酸和强碱的中和反应的活化能接近于零,所以反应速率很高 | |
| B. | 过程的自发性既能用于判断过程的方向,也能用于判断过程发生的速率 | |
| C. | 电解质溶液导电的过程中,一定发生了电解质溶液的电解 | |
| D. | 溶解度较小的BaSO4在一定条件下也可以转化为溶解度略大的BaCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
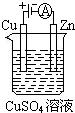 (1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y元素最高价氧化物对应水化物化学式H2YO4 | |
| B. | 原子半径由大到小的顺序为:Y>Z>X | |
| C. | X与W形成的两种化合物中,阴、阳离子物质的量之比均为1:2 | |
| D. | X、Z两种元素的气态氢化物中,Z的气态氢化物较稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 碱性: Mg (OH)2> Cu(OH)2 | 第一电离能:O< N | 熔点: MgS< MgO | 稳定性: H2S< H2O |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H6和C4H10一定是同系物 | |
| B. | C2H4和C4H8一定是同系物 | |
| C. | 相对分子质量相等的两种物质,不一定是同分异构体 | |
| D. | 烯烃各同系物含碳的质量分数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
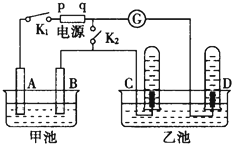 在如图均用石墨作电极的电解池中,甲池中为500mL含某一溶质的蓝色溶液,乙池中为500mL稀硫酸,闭合K1,断开K2进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,立即停止电解,取出A电极,洗涤、干燥、称量,电极质量增重1.6g.请回答下列问题:
在如图均用石墨作电极的电解池中,甲池中为500mL含某一溶质的蓝色溶液,乙池中为500mL稀硫酸,闭合K1,断开K2进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,立即停止电解,取出A电极,洗涤、干燥、称量,电极质量增重1.6g.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H4、C3H6 | B. | C2H4、C4H8 | C. | C3H4、C4H8 | D. | C3H4、C3H6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com