
(13分)工业上用重晶石(BaSO4)制备其他钡盐的常用方法主要有高温煅烧还原法、沉淀转化法等。
I.高温煅烧还原法
工业上利用重晶石高温煅烧还原法制备BaCl2的工艺流程图如下:
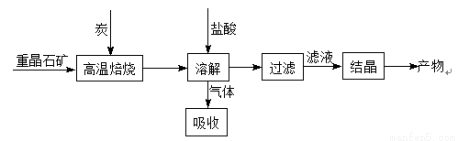
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查表得:
BaSO4(s) + 4C(s) 4CO(g) + BaS(s) △H1 = + 571.2 kJ·mol-1 ①
4CO(g) + BaS(s) △H1 = + 571.2 kJ·mol-1 ①
BaSO4(s) + 2C(s) 2CO2(g) + BaS(s) △H2 = + 226.2 kJ·mol-1 ②
2CO2(g) + BaS(s) △H2 = + 226.2 kJ·mol-1 ②
(1)气体用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为: 。
(2)反应C(s) + CO2(g) 2CO(g)的△H= kJ·mol-1。
2CO(g)的△H= kJ·mol-1。
(3)实际生产中必须加入过量的炭,同时还要通入空气,其目的可能是 。
II.沉淀转化法
(4)已知KSP(BaSO4) =1.0×10-10,KSP(BaCO3)=2.5×10-9。某同学设想用饱和Na2CO3溶液和盐酸将BaSO4转化成BaCl2,若用10 L Na2CO3溶液一次性溶解并完全转化1.0 mol BaSO4(溶液体积变化可忽略不计), 则该转化过程的离子方程式为 ; 反应的平衡常数K= ;Na2CO3溶液的最初浓度不得低于 。
(1)S2- + H2O 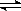 HS- +OH-;HS- + H2O
HS- +OH-;HS- + H2O 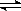 H2S +OH-(写第一步即可)(2分)
H2S +OH-(写第一步即可)(2分)
(2)+ 172.5 ;(2分) (3)使BaSO4得到充分的还原(或提高BaS的产量);①②为吸热反应,炭和氧气反应放热维持反应所需高温。(其他合理答案也给分)(2分)
(4)BaSO4(s) + CO32-(aq) BaCO3(s) + SO42-(3分) 0.04(2分);2.6 mol/L(2分)
BaCO3(s) + SO42-(3分) 0.04(2分);2.6 mol/L(2分)
【解析】
试题分析:(1)硫化钠是强碱弱酸盐,硫离子水解,方程式为S2- + H2O 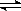 HS- +OH-。
HS- +OH-。
(2)已知BaSO4(s) + 4C(s) 4CO(g) + BaS(s) △H1=+ 571.2 kJ·mol-1 ①,BaSO4(s) + 2C(s)
4CO(g) + BaS(s) △H1=+ 571.2 kJ·mol-1 ①,BaSO4(s) + 2C(s) 2CO2(g) + BaS(s) △H2 = + 226.2 kJ·mol-1 ②,则根据盖斯定律可知(①—②)÷2即可得到反应C(s) + CO2(g)
2CO2(g) + BaS(s) △H2 = + 226.2 kJ·mol-1 ②,则根据盖斯定律可知(①—②)÷2即可得到反应C(s) + CO2(g) 2CO(g)的△H=+ 172.5kJ·mol-1。
2CO(g)的△H=+ 172.5kJ·mol-1。
(3)过量的碳能使BaSO4得到充分的还原(或提高BaS的产量);同时①②为吸热反应,炭和氧气反应放热可以维持反应所需高温,所以实际生产中必须加入过量的炭,同时还要通入空气。
(4)饱和Na2CO3溶液和BaSO4反应的离子方程式为BaSO4(s) + CO32-(aq) BaCO3(s) + SO42-;反应的平衡常数K=
BaCO3(s) + SO42-;反应的平衡常数K= 。当完全转化后溶液中硫酸根的浓度是1mol÷10L=0.1mol/L,所以溶液中碳酸根的浓度是0.1mol/L÷0.04=2.5mol/L。生成1mol碳酸钡消耗1mol碳酸钠,所以碳酸钠的起始浓度不低于
。当完全转化后溶液中硫酸根的浓度是1mol÷10L=0.1mol/L,所以溶液中碳酸根的浓度是0.1mol/L÷0.04=2.5mol/L。生成1mol碳酸钡消耗1mol碳酸钠,所以碳酸钠的起始浓度不低于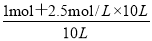 =2.6mol/L。
=2.6mol/L。
考点:考查物质制备工艺流程图的分析以及溶解平衡的应用


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014-2015学年湖南省郴州市高三第二次月考理综化学试卷(解析版) 题型:选择题
现有CuO和Fe3O4的混合物7.6g,向其中加入1mol/L的H2SO4溶液100 mL恰好完全反应,若将15.2 g该混合物用足量CO还原,充分反应后剩余固体质量为:
A.13.6g B.12g C.6g D.3.2 g
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省唐山市高三上学期期末理综化学试卷(解析版) 题型:选择题
有机物C4H8Cl2的结构中只含有一个甲基的同分异构体有几种(不考虑立体异构)
A.3 B.4 C.7 D.8
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省泉州市高三上学期期末化学试卷(解析版) 题型:选择题
反应CO2(g)+2NH3(g) CO(NH2)2(s)+H2 O(g) △H<0,达到平衡时,下列说法正确的是
CO(NH2)2(s)+H2 O(g) △H<0,达到平衡时,下列说法正确的是
A.加入催化剂,平衡常数不变
B.减小容器体积,正、逆反应速率均减小
C.增大CO(NH2)2的量,CO2的转化率减小
D.降低温度,平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省泉州市高三上学期期末化学试卷(解析版) 题型:选择题
下列关于有机化合物的说法正确的是
A.糖类、油脂、蛋白质都属于天然高分子化合物
B.分子式为C2 H6 O、C4 H10的有机物都有2种同分异构体
C.乙烯和苯都能使酸性KMnO4溶液褪色
D.可用热的NaOH溶液除去乙酸乙酯中的乙酸杂质
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省等三校高三上学期联考化学试卷(解析版) 题型:选择题
硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如图,下列说法正确的是

A.283 K时,图中a点对应的溶液是不饱和溶液
B.三个不同温度下,363 K时Ksp(SrSO4)最大
C.温度一定时,Ksp(SrSO4)随c(SO42-)的增大而减小
D.283 K下的SrSO4饱和溶液升温到363 K后变为不饱和溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省等三校高三上学期联考化学试卷(解析版) 题型:选择题
根据下列化学实验事实得出的结论一定正确的是
A.向某无色溶液中先加入氯化钡溶液,生成白色沉淀,再加入足量盐酸,沉淀不溶解。结论:该溶液中含有SO42-
B.向某无色溶液中加入足量盐酸,产生能使澄清石灰水变浑浊的气体。结论:该溶液中含有CO32-或HCO3-
C.向1 mL浓度均为0.05 mol/L的NaCl、NaI混合溶液中滴加2滴0.01 mol /L的AgNO3溶液,振荡,沉淀呈黄色。结论:Ksp(AgCl)<Ksp(AgI)
D.向某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝。结论:该溶液中有NH4+
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省宁德市高三上学期期末化学试卷(解析版) 题型:选择题
正、负极都是碳材料的双碳性电池,电池充、放电过程为2nC+LiA  CnA+LiCn,充电时Li+、A-分别吸附在两极上形成LiCn和CnA(如图所示),下列说法正确的是
CnA+LiCn,充电时Li+、A-分别吸附在两极上形成LiCn和CnA(如图所示),下列说法正确的是
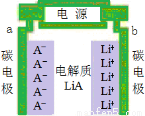
A.a是电池的负极
B.放电时,A-离子向b极移动
C.放电时,负极的电极反应式是nC-e-+A-= CnA
D.充电时,电解质中的离子浓度保持不变
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省咸宁市高二上学期期末考试化学(B)试卷(解析版) 题型:选择题
被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰。在纸内的离子“流过”水和氢氧化锌组成的电解液。电池总反应为:
Zn + 2 MnO2 + 2H2O 2MnOOH + Zn (OH)2。下列说法正确的是
A.该电池的正极为锌
B.该电池反应中二氧化锰起催化剂作用
C.当 0.l mol Zn 完全反应时,流经电解液的电子的物质的量为0.2mol
D.电池正极反应式为: 2MnO2 + 2H2O + 2e- 2MnOOH + 2OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com