
 ��A�ĺ��б�����ͬ���칹�壨��A�⣩��7�֣�
��A�ĺ��б�����ͬ���칹�壨��A�⣩��7�֣�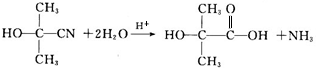 ��
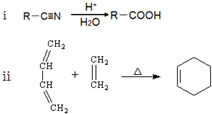
��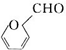 ����һ����Ҫ�Ļ���ԭ�ϣ���ͬ��ȩ�뱽�ӷ�Ӧ���ɷ�ȩ��֬����Ҳ���뱽�ӷ�Ӧ���ɿ�ȩ��֬��д���÷�Ӧ�Ļ�ѧ����ʽ��
����һ����Ҫ�Ļ���ԭ�ϣ���ͬ��ȩ�뱽�ӷ�Ӧ���ɷ�ȩ��֬����Ҳ���뱽�ӷ�Ӧ���ɿ�ȩ��֬��д���÷�Ӧ�Ļ�ѧ����ʽ�� ��
�� ��G
��G ��
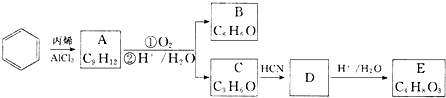
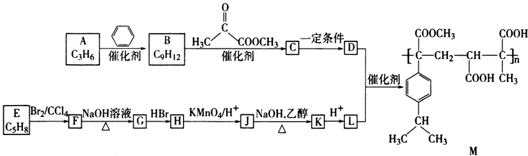
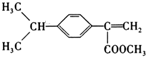
�� ���� AΪ����ͬϵ���һ�ȴ�����5�֣�����A�ķ���ʽ��֪��AΪ �������ϩ�����ӳɷ�Ӧ����A��C��D��E�ĺ˴Ź�������ͼ�У���ĸ����ֱ�Ϊ1��2��3������C�ķ���ʽ��֪��CΪ
�������ϩ�����ӳɷ�Ӧ����A��C��D��E�ĺ˴Ź�������ͼ�У���ĸ����ֱ�Ϊ1��2��3������C�ķ���ʽ��֪��CΪ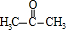 ��C��HCN�����ӳɷ�Ӧ����DΪ
��C��HCN�����ӳɷ�Ӧ����DΪ ������E�ķ���ʽ�Լ�������E�ֱ���������Na��������NaHCO3��Һ��Ӧ������ͬ�����£����ɵ�����������ͬ��֪��D�����������·���ˮ���EΪ
������E�ķ���ʽ�Լ�������E�ֱ���������Na��������NaHCO3��Һ��Ӧ������ͬ�����£����ɵ�����������ͬ��֪��D�����������·���ˮ���EΪ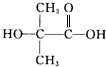 ���Ƚ�A��C�Ľṹ�����B�ķ���ʽ��֪BΪ
���Ƚ�A��C�Ľṹ�����B�ķ���ʽ��֪BΪ ��
��
��� �⣺AΪ����ͬϵ���һ�ȴ�����5�֣�����A�ķ���ʽ��֪��AΪ �������ϩ�����ӳɷ�Ӧ����A��C��D��E�ĺ˴Ź�������ͼ�У���ĸ����ֱ�Ϊ1��2��3������C�ķ���ʽ��֪��CΪ
�������ϩ�����ӳɷ�Ӧ����A��C��D��E�ĺ˴Ź�������ͼ�У���ĸ����ֱ�Ϊ1��2��3������C�ķ���ʽ��֪��CΪ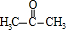 ��C��HCN�����ӳɷ�Ӧ����DΪ
��C��HCN�����ӳɷ�Ӧ����DΪ ������E�ķ���ʽ�Լ�������E�ֱ���������Na��������NaHCO3��Һ��Ӧ������ͬ�����£����ɵ�����������ͬ��֪��D�����������·���ˮ���EΪ
������E�ķ���ʽ�Լ�������E�ֱ���������Na��������NaHCO3��Һ��Ӧ������ͬ�����£����ɵ�����������ͬ��֪��D�����������·���ˮ���EΪ ���Ƚ�A��C�Ľṹ�����B�ķ���ʽ��֪BΪ
���Ƚ�A��C�Ľṹ�����B�ķ���ʽ��֪BΪ ��
��
��1��EΪ �����еĹ��������Ȼ����ǻ����ǻ����Ȼ�����Na��Ӧ����������1molE��Ӧ��������1mol���Ȼ���̼�����Ʒ�Ӧ���ɶ�����̼��1molE��Ӧ����1mol������̼���ʵõ�������������̼������ڱ���¾�Ϊ22.4L��
�����еĹ��������Ȼ����ǻ����ǻ����Ȼ�����Na��Ӧ����������1molE��Ӧ��������1mol���Ȼ���̼�����Ʒ�Ӧ���ɶ�����̼��1molE��Ӧ����1mol������̼���ʵõ�������������̼������ڱ���¾�Ϊ22.4L��
�ʴ�Ϊ���Ȼ����ǻ���22.4L��
��2��C��D�ķ�Ӧ�����Ǽӳɷ�Ӧ���ʴ�Ϊ���ӳɷ�Ӧ��
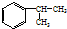
��3��A�Ľṹ��ʽΪ ��A�ĺ��б�����ͬ���칹�壨��A�⣩Ϊ����������һ������Ϊ-CH2CH2CH3����������������Ϊ-CH3��-CH2CH3�����ڼ�����֣�����������-CH3�����ݶ�����һ��ԭ���֪��3�ֽṹ�����Թ���7�֣�
��A�ĺ��б�����ͬ���칹�壨��A�⣩Ϊ����������һ������Ϊ-CH2CH2CH3����������������Ϊ-CH3��-CH2CH3�����ڼ�����֣�����������-CH3�����ݶ�����һ��ԭ���֪��3�ֽṹ�����Թ���7�֣�
�ʴ�Ϊ�� ��7��
��7��
��4��D��E��Ӧ�Ļ�ѧ����ʽ��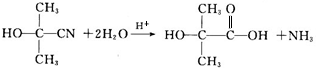 ��
��
�ʴ�Ϊ��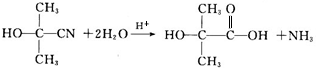 ��
��
��5����ȩ��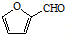 ����һ����Ҫ�Ļ���ԭ�ϣ���ͬ��ȩ�뱽�ӷ�Ӧ���ɷ�ȩ��֬����Ҳ���뱽�ӷ�Ӧ���ɿ�ȩ��֬���÷�Ӧ�Ļ�ѧ����ʽΪ
����һ����Ҫ�Ļ���ԭ�ϣ���ͬ��ȩ�뱽�ӷ�Ӧ���ɷ�ȩ��֬����Ҳ���뱽�ӷ�Ӧ���ɿ�ȩ��֬���÷�Ӧ�Ļ�ѧ����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��6��EΪ��CH3��2COHCOOH��E�ж�����ˮ�������F������Ԫ��״�ṹ��G��һ�־����߷��Ӳ��ϣ���FΪ ��GΪ
��GΪ ��
��
�ʴ�Ϊ�� ��
�� ��
��
���� ���⿼���л�����ƶϣ���Ŀ�Ѷ��еȣ��ؼ���ȷ��A�Ľṹ������������Ϣ������ʵĹ����ŵı仯�����ƶϣ�ע����չ����ŵ����ʣ�


 �Ͻ�ƽ��У����ϵ�д�
�Ͻ�ƽ��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
��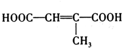 ��д�ṹ��ʽ����
��д�ṹ��ʽ����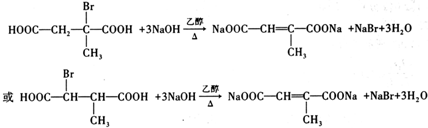 ��
��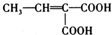 ��д�ṹ��ʽ����
��д�ṹ��ʽ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
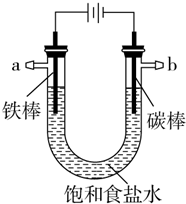 ��̼�����������������������NaCl��Һ����ʼԼ20���������������ɫ���ǣ�Ȼ��ʼ���ֻ���ɫ���ǣ�������ɽ϶�ĺ��ɫ����������˵����ȷ���ǣ�������
��̼�����������������������NaCl��Һ����ʼԼ20���������������ɫ���ǣ�Ȼ��ʼ���ֻ���ɫ���ǣ�������ɽ϶�ĺ��ɫ����������˵����ȷ���ǣ�������| A�� | �����缫��Ӧʽ��Fe-3e-�TFe3+ | |
| B�� | ˮ������������ɫ������ΪNaCl���� | |
| C�� | ����ɫ������Fe��OH��2 | |
| D�� | ���ŵ��Ľ��У���Һ�������Ա�ɼ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
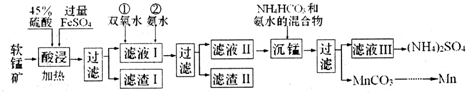
| ���� | Mn��OH��2 | Fe��OH��2 | Fe��OH��3 | Al��OH��3 |
| Ksp | 10-13 | 10-17 | 10-39 | 10-33 |
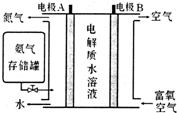
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
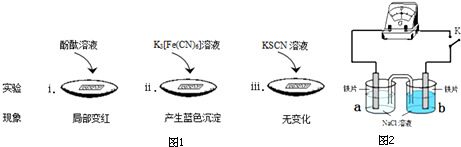
| ʵ�� | a | b | ָ��ƫת���� |
| �� | 0.1% | 0.01% | ���� |
| �� | 0.1% | 3.5% | ���� |
| �� | 3.5% | ������Һ | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaHCO3��Һ�ʼ��Ե�ԭ����HCO3-��ˮ��̶ȴ��ڵ���̶� | |
| B�� | ����CaCl2�ٽ���HCO3-�ĵ��� | |
| C�� | ��Ӧ�����ӷ���ʽ��2HCO3-+Ca2+�TCaCO3��+H2CO3 | |
| D�� | ��Ӧ�����Һ�д��ڣ�c��Na+��+2c��Ca2+��=c��HCO3-��+2c��CO32-��+c��Cl-��+c��H2CO3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | HRΪǿ�� | |
| B�� | a��b������ʾ��Һ��ˮ�ĵ���̶���ͬ | |
| C�� | b����Һ��c�� NH4+����c�� R-����c��OH-����c��H+�� | |
| D�� | a��c�������Һ����c��H+����c��OH-��=Kw=l.0��l0-14 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1mol����1molCl2��ַ�Ӧ��ת�Ƶ�����Ϊ3NA | |
| B�� | ���³�ѹ�£�2gD216O �к������������������������������ | |
| C�� | 14g ����ʽΪCnH2n �ģ�n��2�������к��е�C=C ����Ŀһ��Ϊ$\frac{{N}_{A}}{n}$ | |
| D�� | �ں�Al3+����ΪNA��AlCl3��Һ�У�Cl-����Ϊ3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
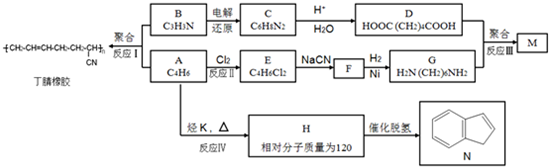
 ��
�� ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com