
| A. | 将Na2O2固体投入滴加了少许酚酞的蒸馏水中,溶液先变红后褪色 | |
| B. | 向胆矾晶体(CuSO4•5H2O)滴加浓硫酸,晶体由蓝色变为黑色 | |
| C. | 用玻璃棒蘸取浓硝酸滴加到pH试纸上,试纸先变红后变成白色 | |
| D. | 将SO2通入品红溶液中,溶液颜色褪去,加热后又变成红色 |
分析 A.过氧化钠与水反应生成氢氧化钠溶液,所以其水溶液都呈碱性,加入酚酞变红,由于过氧化钠具有氧化性,可使溶液褪色而漂白;
B.胆矾失去结晶水生成硫酸铜;
C.依据浓硝酸的酸性和强氧化性解答;
D.依据二氧化硫具有漂白性,且其漂白性具有不稳定性解答.
解答 解:A.过氧化钠与水反应生成氢氧化钠溶液,所以其水溶液都呈碱性,加入酚酞变红,由于过氧化钠具有氧化性,可使溶液褪色而漂白,所以将Na2O2固体投入滴加了少许酚酞的蒸馏水中,溶液先变红后褪色,故A正确;
B.向胆矾晶体(CuSO4•5H2O)滴加浓硫酸,浓硫酸具有吸水性,是晶体由蓝色变为白色,故B错误;
C.浓硝酸具有酸性能够使pH试纸变红,浓硝酸具有强氧化性,能够使变红的试纸褪色,故C正确;
D.二氧化硫具有漂白性,且其漂白性具有不稳定性,所以将SO2通入品红溶液中,溶液颜色褪去,加热后又变成红色,故D正确;
故选:B.
点评 本题考查了元素化合物知识,熟悉过氧化钠、浓硝酸、浓硫酸、二氧化硫的性质是解题关键,题目难度不大,掌握基础是解题关键.


 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:选择题
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.071 | 0.099 |
| 主要化合价 | +2 | +3 | +6、-2 | -1 | -1 |
| A. | A、B简单离子半径大小关系为:B>A | |
| B. | D、E形成的简单离子的还原性:E>D | |
| C. | 气态氢化物的稳定性:D<C | |
| D. | 最高价氧化物对应的水化物的酸性:C>E |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色强碱性溶液中可能大量存在 Al3+、NH4+、Cl?、S2? | |
| B. | 酸性溶液中可能大量存在 Na+、ClO?、SO42?、I? | |
| C. | 弱碱性溶液中可能大量存在 Na+、K+、Cl?、CO32? | |
| D. | 中性溶液中可能大量存在 Ba2+、K+、Cl?、SO42? |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
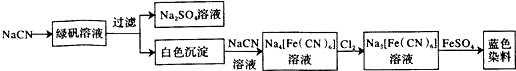
.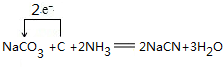 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
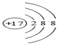 .
. ,ZW与水反应放出气体的化学方程式为NaH+H2O═NaOH+H2↑.
,ZW与水反应放出气体的化学方程式为NaH+H2O═NaOH+H2↑.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,,固体甲与水的离子方程式2Na2O2+2H2O=4Na++4OH-+O2↑,0.5mol的固体甲与CO2反应转移的电子数目0.5NA.
,,固体甲与水的离子方程式2Na2O2+2H2O=4Na++4OH-+O2↑,0.5mol的固体甲与CO2反应转移的电子数目0.5NA.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 正极材料 | Zn | C | Zn | Mg |
| 负极材料 | Cu | Zn | Ag | Zn |
| 电解质溶液 | CuCl2 | CuSO4 | CuSO4 | CuCl2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CH3CH=CH2和CH2=CH2的最简式相同 | |
| B. | 二氯甲烷没有同分异构体 | |
| C. | 丁二烯和丁烯为同系物 | |
| D. | 正戊烷、异戊烷、新戊烷的沸点逐渐升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L0.1mol/L HCl溶液中含有0.1NA个HCl分子 | |
| B. | 23gNa在空气中燃烧生成Na2O2时转移电子数目为2NA | |
| C. | 28gCO和N2的混合气体中电子数目为14NA | |
| D. | 11.2LCO2含氧原子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com