
科目:高中化学 来源: 题型:
下列反应既是氧化还原反应,又是吸热反应的是
A.灼热的炭与CO2反应 B.Ba(OH)2·8H2O与NH4Cl的反应
C. 铝片与稀硫酸反应 D.甲烷在O2中的燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)按系统命名法命名.
①有机物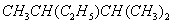 的名称是 。
的名称是 。
(2)写出下列各种有机物的结构简式
①2,3-二甲基-4-乙基已烷 ;
②支链只有一个乙基且式量最小的烷烃 ;
③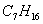 的同分异构体中具有“手性碳原子”的有 种,写出其中一种的名称 。
的同分异构体中具有“手性碳原子”的有 种,写出其中一种的名称 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )
| 选项 | 叙述I | 叙述II |
| A | 干燥的Cl2通入品红溶液中,品红褪色 | 干燥的Cl2具有漂白性 |
| B | NH4Cl受热易分解 | 用加热法除去 NaCl中的NH4Cl |
| C | Na2O2使酚酞溶液变红 | Na2O2使品红溶液褪色 |
| D | CaCO3难溶于水 | CO2通入CaCl2溶液中产生白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
己知X、Y、Z、W、N、U、V是短周期的主族元素,原子序数依次增大。X与N同主族,且与W都能形成A2B、A2B2型化合物;Z、W的单质常温下均为无色气体;Y原子的L层电子数是K层电子数的2倍;U原子的最外层电子数是其电子层数的2倍,试回答下列问题:
(1)YW2的电子式 ;Z的氢化物结构式为 ;写出U元素在周期表中的位置 。
(2)原子半径:U V(填>、<或=,下同);气态氢化物的水溶液的酸性:U V。
(3)写出UW2与V元素的单质在水溶液中反应的化学方程式是 。
(4)由X、Z组成的一种化合物化学式为ZX5,其各原子均达到同周期稀有气体原子的稳定结构,该物质属于 (填“离子”或“共价”)化合物。
(5)X、Y、Z、W四种元素(按顺序)可组成原子个数比为5:1:1:3的化合物,该化合物的稀溶液与足量氢氧化钠溶液在加热条件下反应的离子方程式为:
。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于氢键的下列说法中正确的是( )
A.每个水分子内含有两个氢键
B.在水蒸气、水和冰中都含有氢键
C.HF的稳定性很强,是因为其分子间能形成氢键
D.分子间能形成氢键使物质的熔点和沸点升高
查看答案和解析>>
科目:高中化学 来源: 题型:
铅蓄电池是广泛应用于汽车、柴油机车等的启动电源。产生电能时的电极反应分别为:
Pb+SO42―–2e―=PbSO4 ①
PbO2+4H++SO42―+2e―=PbSO4+2H2O ②
下列有关铅蓄电池的说法不正确的是: ( )
A.①式表示负极反应,②式表示正极反应
B.铅蓄电池的电解质溶液是硫酸溶液,在放电过程中,它的浓度逐渐降低
C.铅蓄电池在放电时,电子从Pb通过导线流向PbO2
D.铅蓄电池在充电时,原来负极发生的反应是:Pb+SO42―–2e―=PbSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨是人类研究的重要课题,目前工业合成氨的原理为:
合成氨是人类研究的重要课题,目前工业合成氨的原理为:
N2(g)+3H2(g) 2NH3(g)△H=-93.0kJ•mol-1,在3个2L的密闭容器中,使用相同的催化剂,按不同方式投入反应物,分别进行反应:
2NH3(g)△H=-93.0kJ•mol-1,在3个2L的密闭容器中,使用相同的催化剂,按不同方式投入反应物,分别进行反应:
相持恒温、恒容,测的反应达到平衡时关系数据如下:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 3molH2、2molN2 | 6molH2、4molN2 | 2mol NH3 |
| 达到平衡的时间/min | 6 | 8 | |
| 平衡时 N2的体积密度 | C1 | 1.5 | |
| 混合气体密度/g·L-1 |
|
| |
| 平衡常数/ L2·mol-2 | K甲 | K乙 | K丙 |
(1)下列各项能说明该反应已到达平衡状态的是 (填写序号字母)
a.容器内H2、N2 、NH3的浓度只比为1:3:2 b.容器内压强保持不变
c.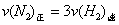 d.混合气体的密度保持不变
d.混合气体的密度保持不变
e.混合气体的平均相对分子质量不变
(2)容器乙中反应从开始到达平衡的反应速度为 =
=
(3)在该温度下甲容器中反应的平衡常数K (用含C1的代数式表示)
(4)分析上表数据,下列关系正确的是 (填序号):
a. b.
b. c.
c. 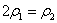 d.
d.
(5)另据报道,常温、常压下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,生成NH3和O2。已知:H2的燃烧热△H=-286KJ/mol,则由次原理制NH3反应的热化学方程式为
(6)希腊阿里斯多德大学的George Mamellos和Michacl Stoukides,发明了一种合成氨的新方法,在常压下,把氢气和用氨气稀释的氮气分别通入一个加热到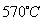 的电解池,李勇能通过的氢离子的多孔陶瓷固体作电解质,氢气和氮气在电极上合成了氨,转化率达到78%,在电解法合成氨的过程中,应将H2不断地通入 极,该电极反应式为 。
的电解池,李勇能通过的氢离子的多孔陶瓷固体作电解质,氢气和氮气在电极上合成了氨,转化率达到78%,在电解法合成氨的过程中,应将H2不断地通入 极,该电极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com