
【题目】某溶液中含有的离子可能是K+、Ba2+、Al3+、Mg2+、AlO2-、CO32-、SiO32-、Cl-中的几种,现进行如下实验:
①取少量溶液,加氢氧化钠溶液过程中无沉淀生成;
②另取少量原溶液,逐滴加入5mL0.2mol·L-1盐酸,产生的现象是:开始产生沉淀并逐渐增多,沉淀量基本不变后产生气体,最后沉淀逐渐减少至消失;
③在上述②沉淀消失后的溶液中,再加入足量的硝酸银溶液可得到沉淀0.287g。
下列说法中正确的是( )
A.该溶液中一定不含Ba2+、Mg2+、Al3+、SiO32-、Cl-
B.该溶液中一定含有K+、AlO2-、CO32-、Cl-
C.该溶液是否有K+需做焰色反应实验(透过蓝色钴玻璃片)
D.可能含有Cl-
【答案】B
【解析】
①加氢氧化钠溶液过程中无沉淀生成,说明溶液中一定不存在A13+、Mg2+;②另取少量原溶液,逐滴加入5mL0.2molL-1盐酸,开始产生沉淀并逐渐增多,沉淀量基本不变后产生气体,最后沉淀逐渐减少至消失,产生和溶解的沉淀为氢氧化铝,产生的气体为二氧化碳,说明溶液中存在AlO2-、CO32-,所以一定不存在SiO32-、Ba2+,根据溶液呈电中性,溶液中一定存在K+;③在上述②沉淀消失后的溶液中,再加入足量的硝酸银溶液可得到沉淀0. 287g,沉淀为AgCl,物质的量为![]() =0.002mol>n(HCl)=0.005L×0.2mol/L=0.001mol,所以原溶液中一定存在0.001molCl-,据此分析解答。
=0.002mol>n(HCl)=0.005L×0.2mol/L=0.001mol,所以原溶液中一定存在0.001molCl-,据此分析解答。
A.根据以上分析可知,溶液中一定不存在Ba2+、Mg2+、A13+、SiO32-,一定存在Cl-,故A错误;
B.由上述分析可知:该溶液中一定含有K+、AlO2-、CO32-、Cl-,故B正确;
C.根据溶液的电中性可以判断,溶液中一定存在K+,不需要通过焰色反应判断K+是否存在,故C错误;
D.根据分析可知,原溶液中一定存在Cl-,故D错误;
故选B。


科目:高中化学 来源: 题型:
【题目】下列化学方程式中,不能正确表达反应颜色变化的是
A. 向CuSO4溶液中加入足量Zn粉,溶液蓝色消失Zn+CuSO4![]() Cu+ZnSO4
Cu+ZnSO4
B. 澄清的石灰水久置后出现白色固体Ca(OH)2+CO2![]() CaCO3↓+H2O
CaCO3↓+H2O
C. Na2O2在空气中放置后由淡黄色变为白色2Na2O2![]() 2Na2O+O2↑
2Na2O+O2↑
D. 向Mg(OH)2悬浊液中滴加足量FeCl3溶液出现红褐色沉淀3Mg(OH)2+2FeCl3![]() 2Fe(OH)3+3MgCl2
2Fe(OH)3+3MgCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,有甲、乙两个密闭容器,甲容器的体积为1 L,乙容器的体积为2 L,分别向甲、乙两容器中加入6 mol A和3 mol B,发生反应如下:3A(g)+bB(g)![]() 3C(g)+2D(g) ΔH<0;4 min时甲容器内的反应恰好达到平衡,A的浓度为2.4 mol/L,B的浓度为1.8 mol/L;t min时乙容器内的反应达平衡,B的浓度为0.8 mol/L。根据题给信息回答下列问题:
3C(g)+2D(g) ΔH<0;4 min时甲容器内的反应恰好达到平衡,A的浓度为2.4 mol/L,B的浓度为1.8 mol/L;t min时乙容器内的反应达平衡,B的浓度为0.8 mol/L。根据题给信息回答下列问题:
(1)甲容器中反应的平均速率v(B)=____,化学方程式中计量数b=____;
(2)乙容器中反应达到平衡时所需时间t___4min(填“大于”、“小于”或“等于”),原因是_____;
(3)若要使甲、乙容器中B的平衡浓度相等,可以采取的措施是___;
A. 保持温度不变,增大甲容器的体积至2L
B. 保持容器体积不变,使甲容器升高温度
C. 保持容器压强和温度都不变,向甲中加入一定量的A气体
D. 保持容器压强和温度都不变,向甲中加入一定量的B气体
(4)写出平衡常数表达式K=____,并计算在T℃时的化学平衡常数K=____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某地环保部门将收集到的一定量酸雨试样分成甲、乙、丙、丁四份,进行如图所示的实验探究。
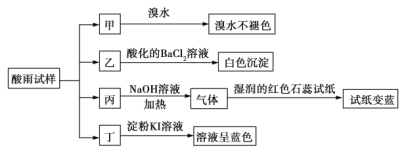
已知酸雨试样中可能含有下表所示的某些离子:
阳离子 |
|
阴离子 |
|
请回答下列问题:
(1)![]() 是______,
是______,![]() 是______。
是______。
(2)可能存在的阴离子是______,能证明该阴离子是否存在的简单实验操作为______。
(3)写出丁试样中滴加淀粉![]() 溶液所发生反应的离子方程式:______。
溶液所发生反应的离子方程式:______。
(4)某次降雨收集到![]() 雨水,向雨水中滴加
雨水,向雨水中滴加![]() 的
的![]() 溶液,充分反应后测得溶液中
溶液,充分反应后测得溶液中![]() ,再向该溶液中加入足量的
,再向该溶液中加入足量的![]() 溶液,经过滤、蒸干、称重,测得沉淀的质量为
溶液,经过滤、蒸干、称重,测得沉淀的质量为![]() 。假设雨水的酸性仅由
。假设雨水的酸性仅由![]() 和
和![]() 的排放所致,则排放到空气中的
的排放所致,则排放到空气中的![]() 和
和![]() 的物质的量之比约为______(不考虑
的物质的量之比约为______(不考虑![]() 的相互反应)。
的相互反应)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.浓硫酸是一种干燥剂,能够干燥氢气、氧气、![]() 、
、![]() 等气体
等气体
B.浓硫酸与单质硫反应的化学方程式为![]() ,在此反应中,浓硫酸既表现出强氧化性又表现出酸性
,在此反应中,浓硫酸既表现出强氧化性又表现出酸性
C.把足量铜粉投入到含![]() 的浓硫酸中,得到气体的体积为
的浓硫酸中,得到气体的体积为![]() (标准状况下)
(标准状况下)
D.常温下能够用铁、铝容器盛放浓硫酸,是因为浓硫酸的强氧化性使铁、铝钝化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在200℃,101kPa下,氢气与碘蒸气混合发生应:H2(g)+I2(g)![]() 2HI(g),则下列叙述正确的是( )
2HI(g),则下列叙述正确的是( )
A.反应达平衡后,增大压强(缩小容器体积),混合气体颜色不变
B.由反应需在200℃进行可推测该反应是吸热反应
C.反应达平衡后,保持容器体积不变,充入大量I2蒸气可提高H2的转化率
D.当v(H2)生成:v(HI)生成=2:1时,反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组设计用铁粉将NO还原为N2(同时生成FeO),下列说法不正确的是
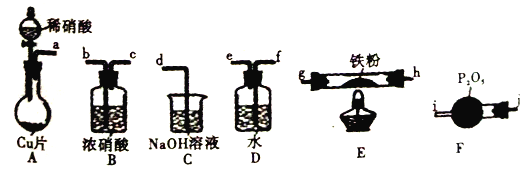
已知:①浓硝酸可氧化NO;②NaOH溶液能吸收NO2,不吸收NO。
A. 装置的连接顺序为a![]() f
f![]() e
e![]() j
j![]() i
i![]() h
h![]() g(或g
g(或g![]() h)
h)![]() b
b![]() c
c![]() d
d
B. 装置E中发生的化学方程式为2NO+2Fe![]() 2FeO+N2
2FeO+N2
C. 装置D的作用是吸收挥发出来的硝酸和产生NO2
D. 装置B的作用是干燥,防止水蒸气进入E中干扰反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼镁泥是一种工业废料,主要成分是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的流程如下:
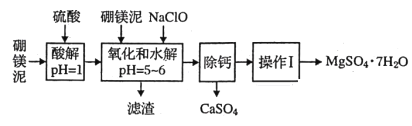
(1)实验中需用1mol/L的硫酸480mL,若用18.4mol/L的浓硫酸来配置,量取浓硫酸时需使用的量筒规格为(_______)。
A 10mL B 20mL C 50mL D 100mL
(2)加入的NaClO可与Mn2+反应:Mn2++ClO-+H2O=MnO2↓+2H++Cl-还有一种离子也会被NaClO氧化,该反应的离子方程式为___________________________;滤渣中除含有氢氧化铁、氢氧化铝外还有_________。
(3)在“除钙”前需检验滤液中Fe3+是否被除尽,简述检验方法_____________________。
(4)已知硫酸镁、硫酸钙的溶解度如下表
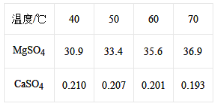
“除钙”是将;硫酸镁和硫酸钙混合溶液中的硫酸钙除去根据上表数据,采取的操作是_______________、趁热过滤、_________、____________,便得到比较纯净的硫酸镁。
(5)实验中提供的硼镁泥共100g,得到的MgSO4·7H2O为172.2g,则MgSO4·7H2O的产率为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com