
科目:高中化学 来源: 题型:阅读理解

| 物质 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
| 沸点/℃ | 57.7 | 12.8 | - | 315 | - |
| 熔点/℃ | -70.0 | -107.2 | - | - | - |
| 升华温度/℃ | - | - | 180 | 300 | 162 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 有机物\物理性质 | 熔点/℃ | 沸点/℃ | 溶解性 |
| 1-萘乙酸 | 134.5 | 285(分解) | 易溶于热水,难溶于冷水,易溶于碱 |
| 萘 | 80.5 | 219.9 | 不溶于热水 |
| 氯乙酸 | 62 | 189 | 溶于水 |
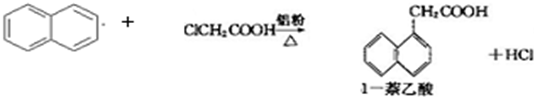
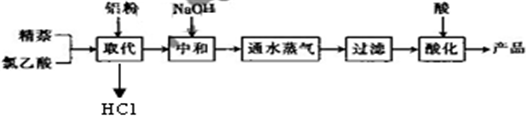
| 实验方法和操作 | 实验目的 |
| 1.把产品放入容器中,加入适量的蒸馏水,加热并充分搅拌; | 溶解1-萘乙酸和氯乙酸、氯化铝等水溶性杂质 溶解1-萘乙酸和氯乙酸、氯化铝等水溶性杂质 |
| 2. 趁热过滤 趁热过滤 |
除去杂质萘; |
| 3. 取滤液 取滤液 ,再过滤,洗涤,干燥. |
得到提纯的产品1-萘乙酸. |
查看答案和解析>>
科目:高中化学 来源:2004全国各省市高考模拟试题汇编·化学 题型:038
将2.000g Na2SO4、Na2CO3和NaNO3的混合物溶于水得溶液A,在A中加入足量未知浓度的BaCl2溶液10.00mL,然后过滤得沉淀B 3.315g和滤液C;在C中加入足量的AgNO3溶液,又生成5.740g沉淀;向B中加入足量稀硫酸,充分反应后,沉淀质量变为3.495g.计算:
(1)氯化钡溶液的物质的量浓度.
(2)原混合物中硝酸钠的质量分数.
查看答案和解析>>
科目:高中化学 来源:顺德区模拟 题型:问答题
| 有机物\物理性质 | 熔点/℃ | 沸点/℃ | 溶解性 |
| 1-萘乙酸 | 134.5 | 285(分解) | 易溶于热水,难溶于冷水,易溶于碱 |
| 萘 | 80.5 | 219.9 | 不溶于热水 |
| 氯乙酸 | 62 | 189 | 溶于水 |
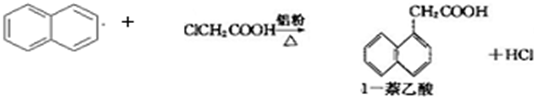
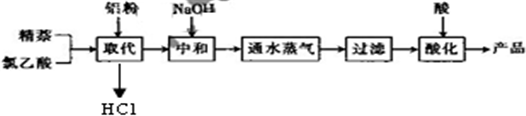
| 实验方法和操作 | 实验目的 |
| 1.把产品放入容器中,加入适量的蒸馏水,加热并充分搅拌; | ______ |
| 2.______ | 除去杂质萘; |
| 3.______,再过滤,洗涤,干燥. | 得到提纯的产品1-萘乙酸. |
查看答案和解析>>
科目:高中化学 来源:2011年广东省佛山市顺德区高考化学模拟试卷(解析版) 题型:解答题
| 有机物\物理性质 | 熔点/℃ | 沸点/℃ | 溶解性 |
| 1-萘乙酸 | 134.5 | 285(分解) | 易溶于热水,难溶于冷水,易溶于碱 |
| 萘 | 80.5 | 219.9 | 不溶于热水 |
| 氯乙酸 | 62 | 189 | 溶于水 |
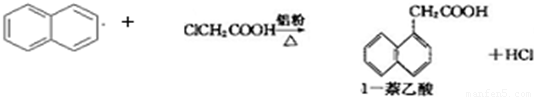
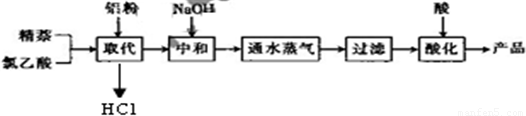
| 实验方法和操作 | 实验目的 |
| 1.把产品放入容器中,加入适量的蒸馏水,加热并充分搅拌; | ______ |
| 2.______ | 除去杂质萘; |
| 3.______,再过滤,洗涤,干燥. | 得到提纯的产品1-萘乙酸. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com