
【题目】下列说法正确的是( )
A.升高体系的温度或增加某一组分的浓度均能增加反应体系中活化分子所占百分数
B.H2+Cl2 ![]() 2HCl反应中化学能只转变为热能
2HCl反应中化学能只转变为热能
C.面粉生产工厂要求严禁烟火是因为面粉有机物颗粒极大,总表面积巨大容易被引燃爆炸
D.高锰酸钾受热分解是一个熵减小的过程
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:
【题目】根据框图分析,下列说法不正确的是
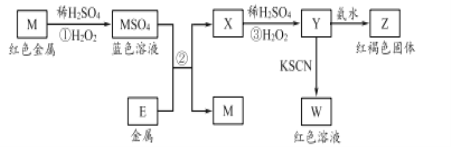
A. 我国是世界上最早使用反应②冶炼金属M的国家
B. M2+的氧化性比E2+的氧化性强
C. 在反应③中若不加稀硫酸,可能观察到红褐色沉淀
D. 在反应①中稀硫酸既表现出氧化性又表现出酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铑基催化剂催化CO加氢合成甲醇(CH3OH)、乙醛(CH3CHO)、乙醇等碳的含氧化合物是近年来化学界比较活跃的研究课题之一。
(1)已知:(ⅰ)CO(g)+2H2(g)![]() CH3OH(g) △H1=-90.1kJ/mol
CH3OH(g) △H1=-90.1kJ/mol
(ⅱ)2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H2=-24.5kJ/mol
CH3OCH3(g)+H2O(g) △H2=-24.5kJ/mol
(ⅲ)C2H5OH(g)![]() CH3OCH3(g) △H3=+50.7kJ/mol
CH3OCH3(g) △H3=+50.7kJ/mol
则由CO催化加氢制备乙醇气体(另一产物为水蒸汽)的热化学反应方程式为________。
(2)直接甲醇燃料电池(DMFC)成本低、效率高,某研究所尝试用DMFC电解处理含氰电镀废水。调节废水pHl0~12.5,电解过程中,CNˉ先被氧化成CNOˉ(两种离子中氮元素均为-3价),再进一步氧化为碳酸盐和N2。
①请写出CNOˉ被氧化的电极反应式________。
②欲处理1m3CNˉ含量为390mg/L的电镀废水,至少需准备________kg甲醇。
(3)在2.0L密闭容器中放入1 molCO与2molH2,在反应温度T1时进行如下反应:
CO(g)+2H2(g)=CH3OH(g),反应时间(t)与容器内气体总物质的量(n)的数据见下表:
时间t/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
总物质的量n/mol | 3.0 | 2.7 | 2.5 | 2.3 | 2.1 | 2.0 | 2.0 |
①在0~5min时段,反应速率v(CH3OH)为________;有利于提高上述反应平衡转化率的条件是________。
A.高温高压 B.低温低压 C.高温低压 D.低温高压
②计算温度T1时反应的平衡常数K1________;T1时达平衡后,改变反应温度为T2,平衡常数增大,则T2________T1(填“大于”“小于”),判断理由是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中符合H+ + OH-=H2O离子反应的是( )
A.稀硫酸与稀氨水B.稀硫酸与氢氧化钡溶液
C.稀硝酸与氢氧化钡溶液D.盐酸与氢氧化铁反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g) + 3H2(g) ![]() 2NH3(g),△H<0,在673 K,30 MPa下,n(NH3)和n(H2)随时间变化的关系如图所示,叙述正确的是( )
2NH3(g),△H<0,在673 K,30 MPa下,n(NH3)和n(H2)随时间变化的关系如图所示,叙述正确的是( )

A.点d(t1时刻)和点e(t2时刻)处n(N2)不一样
B.点c处反应达到平衡
C.点a的正反应速率比点b的大
D.其他条件不变,773 K下反应至t1时刻,n(H2)比上图中d点的值小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列应用与盐类的水解无关的是
A. 明矾用于净水
B. 次氯酸钠常用作消毒剂
C. FeCl3溶液滴入沸水中制Fe(OH)3胶体
D. 用碳酸氢钠和硫酸铝两种溶液可制成泡沫灭火剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法正确的是( )
A.晶体硅可用于制造光导纤维
B.氯氧化钠用来治疗胃酸过多
C.铝制容器可以用来贮运稀硝酸
D.乙烯用作水果的催熟剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列叙述中正确的是( )
A. 已知N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4 kJ·mol-1,当在一定温度压强下向一密闭容器中充入0.5molN2、1.5molH2使其充分反应,其反应放出的热量为46.2 kJ
2NH3(g) △H=-92.4 kJ·mol-1,当在一定温度压强下向一密闭容器中充入0.5molN2、1.5molH2使其充分反应,其反应放出的热量为46.2 kJ
B. 常温常压下,7.1gCl2与足量铁充分反应,转移的电子数为0.2NA
C. 室温下,1LpH=13的NaOH溶液中,由水电离的OH-数目为0.1NA
D. 12g金刚石晶体中含有的碳碳键数目为4NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com