
| A. | 甲烷的燃烧热为890.3 kJ•mol-1,则甲烷燃烧热的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)$?_{30MP}^{500℃}$ 2NH3(g)△H=-38.6 kJ•mol-1 | |
| C. | 已知在120℃、101 kPa下,1 g H2燃烧生成水蒸气放出121 kJ热量,其热化学方程式为H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-242 kJ•mol-1 | |
| D. | 25℃、101 kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ•mol-1,硫酸溶液与氢氧化钾溶液反应的热化学方程式为H2SO4(aq)+2KOH(aq)═K2SO4(aq)+2H2O(l)△H=-57.3 kJ•mol-1 |
分析 A、燃烧热指在25℃,101 kPa时,1 mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热.单位为kJ/mol,生成的水应为液态.
B、0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,生成的氨气的物质的量小于1mol;
C、已知在120℃、101 kPa下,1 g H2燃烧生成水蒸气放出121 kJ热量,2g氢气燃烧生成气态水放热242KJ,标注物质聚集状态和对应反应的焓变得到热化学方程式分析;
D、中和热是生成1mol的水.
解答 解:A、甲烷的标准燃烧热为890.3kJ•mol-1,表示1mol甲烷完全燃烧生成二氧化碳与液态水放出热量为890.3kJ,甲烷燃烧热的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-890.3kJ•mol-1,故A错误;
B、相同条件下的同一可逆反应,正逆反应反应热数值相等,符号相反,0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,生成的氨气的物质的量小于1mol,所以放出热量小于38.6 kJ,故B错误;
C、已知在120℃、101 kPa下,1 g H2燃烧生成水蒸气放出121 kJ热量,2g氢气燃烧生成气态水放热242KJ,其热化学方程式为H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-242 kJ•mol-1,故C正确;
D、中和热是生成1mol的水,而硫酸溶液与氢氧化钾溶液反应中生成2mol的水,故D错误;
故选C.
点评 本题考查了燃烧热、中和热以及热化学方程式中计量数的含义,难度不大,注意把握燃烧热和中和热的概念.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
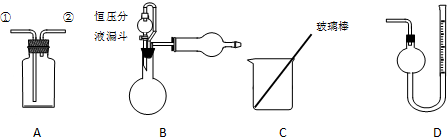
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某温度时,化学反应速率无论用A、C何种物质表示,其数值都是相同的 | |
| B. | 其他条件不变时,升高温度,反应速率加快 | |
| C. | 其他条件不变时,增大压强,反应速率加快 | |
| D. | 若增加或减少A的物质的量,反应速率一定会发生明显的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol任何气体的体积都约是22.4 L | |
| B. | 18 g NH4+含有电子数为10NA | |
| C. | NA个H2SO4分子的质量等于H3PO4的摩尔质量 | |
| D. | 标准状况下,相同体积的O2、HCl含有的分子数都为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1 | B. | 0.2 mol•L-1 | C. | 0.4 mol•L-1 | D. | 0.8 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
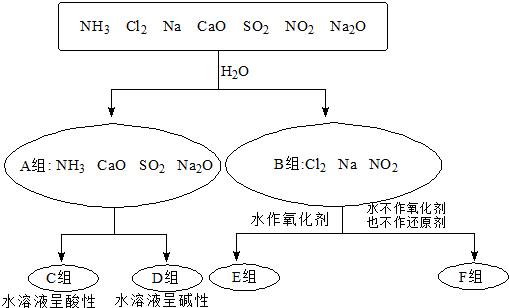
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
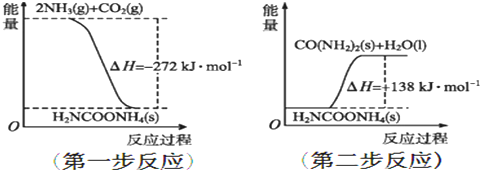
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com