
已知2SO2 (g) + O2 (g) 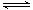 2SO3 (g) ΔH = -197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2 mol SO2和1 mol O2 (乙) 1 mol SO2和0.5 mol O2 (丙) 2 mol SO3 。恒温、恒容下反应达平衡时,下列关系一定正确的是
2SO3 (g) ΔH = -197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2 mol SO2和1 mol O2 (乙) 1 mol SO2和0.5 mol O2 (丙) 2 mol SO3 。恒温、恒容下反应达平衡时,下列关系一定正确的是
A.容器内压强P:P甲=P丙 > 2P乙
B.SO3的质量m:m甲=m丙 > 2m乙
C.c(SO2)与c(O2)之比k:k甲=k丙 > k乙
D.反应放出或吸收热量的数值Q:Q甲=Q丙 > 2Q乙
科目:高中化学 来源: 题型:
室温时,向20 mL 0.1 mol·L-1的醋酸溶液中不断滴入0.1 mol·L-1的NaOH溶液,溶液的pH变化曲线,如图2所示。在滴定过程中,关于溶液中离子浓度大小关系的描述不正确的是( )
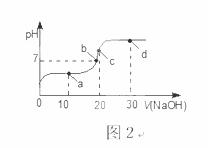
A.a点时:c( CH3COOH)>c( Na+)>c( CH3COO-)>c( H+)>c( OH -)
B.b点时:c( Na+) =c( CH3COO-)>c(H+)=c( OH-)
C.c点时:c(OH-)=c(CH3COOH) +c(H+)
D.d点时:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.1 mol氧为32 g
B.标准状况下,1 mol H2和O2的混合气体的体积约为22.4 L
C.CO2的摩尔质量为44
D.2 mol·L-1的BaCl2溶液中含Cl-的个数为2.408×1024
查看答案和解析>>
科目:高中化学 来源: 题型:
已知热化学方程式:
①C2H2 (g)+5/2O2(g)=2CO2(g)+H2O(l) △H1= _1301.0kJ/mol
②C(s)+O2(g)=CO2(g) △H2= _393.5kJ/mol
③H2(g)+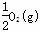 =H2O(l) △H3= _285.8kJ/mol
=H2O(l) △H3= _285.8kJ/mol
则反应④ 2C(s) + H2(g) = C2H2(g)的△H为
A.+621.7kJ/mol B.+1301.0kJ/mol C.-228.2kJ/mol D.+228.2 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下在容积固定的密闭容器中,下列反应达到平衡:
CO(g)+H2O(g) 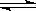 CO2(g)+H2(g)
CO2(g)+H2(g)
| 初始投料比n(CO)n(H2O) | CO转化率 | H2O转化率 |
| 1:1 | 0.5 | 0.5 |
| 1:2 | 0.67 | 0.335 |
| 1:3 | 0.75 | 0.25 |
(1)已知CO和H2的燃烧热分别为283kJ/mol、285.8kJ/mol,H2O(g)=H2O(l)△H= -44kJ/mol,写出CO(g)和H2O(g)反应的热化学方程式 。
(2)该反应的平衡常数为 。该温度下,向该容器中充入1mol CO、3molH2O(g)、2mol CO2、1.5molH2,则起始时该反应速率V正 V逆(填“>”、“<”或“=”)
(3)结合表中数据判断下列说法中正确的是 。
A.增加H2O(g)的量,CO的转化率升高而H2O(g)的转化率降低
B.若CO与H2O(g)的转化率相同,则二者的初始投入量一定相同
C.CO和H2O(g)初始物质的量之比等于二者转化率之比
D.当CO与H2O(g)物质的量之比为1:4时,CO的转化率为0.85
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A. 常温下可用铝制容器贮存稀硝酸B. 钠的化学性质活泼,可从CuSO4溶液中置换出Cu
C. 干燥的氯气具有漂白性 D. 金属钠与氧气反应,条件不同产物不同
查看答案和解析>>
科目:高中化学 来源: 题型:
两份铝屑,第一份与过量的盐酸反应,第二份与过量的NaOH溶液反应,产生氢气的体积 比为1:2,则第一份与第二份铝屑的质量比为 ( )
A.1:1 B.1:2 C.1:3 D.1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
化学反应的实质就是旧键的断裂和新键的形成。欲探讨发生化学反应时分子中化学键在何处断裂的问题,近代科技常用同位素示踪原子法。如有下列反应:
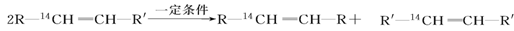

可以推知,物质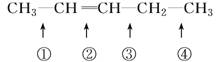 发生此反应时断裂的化学键应是( )
发生此反应时断裂的化学键应是( )
A.①③ B.①④ C.② D.②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com