
| A. | 能使红色石蕊试纸变蓝的溶液中:Na+、K+、CO32-、NO3-、AlO2- | |
| B. | c(H+)=0.1 mol/L的溶液中:Cu2+、Al3+、SO42-、NO3- | |
| C. | 在加入铝粉后能产生氢气的溶液中:NH4+、Fe2+、SO42-、NO3- | |
| D. | 含大量OH-的溶液中:CO32-、Cl-、F-、K+ |
分析 A.能使红色石蕊试纸变蓝色的溶液呈碱性;
B.c(H+)=0.1 mol/L的溶液呈强酸性;
C.加入铝粉能产生氢气的溶液呈强碱性或含有弱氧化性酸;
D.能和氢氧根离子反应的离子不能大量共存.
解答 解:A.能使红色石蕊试纸变蓝色的溶液呈碱性,这几种离子之间不反应且和氢氧根离子不反应,所以能大量共存,故A错误;
B.c(H+)=0.1 mol/L的溶液呈强酸性,这几种离子之间不反应且和氢离子不反应,所以能大量共存,故B错误;
C.加入铝粉能产生氢气的溶液呈强碱性或含有弱氧化性酸,碱性条件下,NH4+、Fe2+不能大量共存,酸性条件下,硝酸根离子和亚铁离子发生氧化还原反应而不能大量共存,且酸性条件下不能生成氢气,故C正确;
D.能和氢氧根离子反应的离子不能大量共存,这几种离子之间不反应且和氢氧根离子不反应,所以能大量共存,故D错误;
故选C.
点评 本题考查离子共存,为高频考点,侧重考查复分解反应及氧化还原反应,注意结合限制性条件分析解答,易错选项是C,注意:硝酸和铝反应不生成氢气,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | 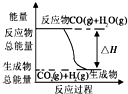 如图表示反应CO(g)+H2O(g)═CO2(g)+H2(g)的△H>0 | |
| B. | 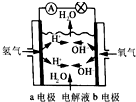 如图为氢氧燃料电池示意图,正、负极通入的气体体积之比为2:1 | |
| C. | 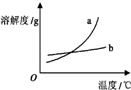 如图表示物质a、b的溶解度曲线,可以用重结晶方法从a、b混合物中提纯a | |
| D. |  如图可以表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,且乙的压强小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 强电解质都是离子化合物,弱电解质都是共价化合物 | |
| B. | 强电解质都是可溶性化合物,弱电解质都是难溶化合物 | |
| C. | 强电解质的水溶液导电能力强,弱电解质导电能力弱 | |
| D. | 强电解质的水溶液中无溶质分子,弱电解质的水溶液中有溶质分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
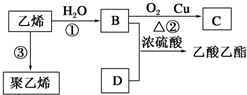
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (CH3)2CHCH(CH3)OH | B. | CH3(CH2)3CH2OH | C. | CH3CH2C(CH3)2OH | D. | (CH3CH2)2CHOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石晶胞(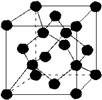 )中平均含有的碳原子数、碘晶体晶胞中平均含有的原子数均为8 )中平均含有的碳原子数、碘晶体晶胞中平均含有的原子数均为8 | |
| B. | 二氧化硅晶体中最小环上的氧原子数、氯化铯晶体中氯离子的配位数均为6 | |
| C. | 锌晶胞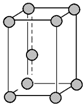 中锌原子的配位数、氯化钠晶体中距离钠离子最近且相等的钠离子数均为12 中锌原子的配位数、氯化钠晶体中距离钠离子最近且相等的钠离子数均为12 | |
| D. | 33g CH≡C-CH=CH-CH3中所含的π键数、12g石墨中所含的碳碳键数均为1.5mol. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
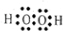 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com