
ĻĀĮŠ·“Ó¦ŹōÓŚĪüČČ·“Ó¦µÄŹĒ( )
| A£®Ģ¼ÓėĖ®ÕōĘųÖĘĖ®ĆŗĘųµÄ·“Ó¦ |
| B£®ÉśŹÆ»ŅŗĶĖ®µÄ·“Ó¦ |
| C£®ŃĪĖįÓėĒāŃõ»ÆÄĘČÜŅŗµÄ·“Ó¦ |
| D£®Ä¾ĢæŌŚŃõĘųÖŠČ¼ÉÕ |
 ¶į¹Ś½š¾ķČ«ÄÜĮ·æ¼ĻµĮŠ“š°ø
¶į¹Ś½š¾ķČ«ÄÜĮ·æ¼ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
·“Ó¦A(g)£«B(g)  C(g)£«D(g)¹ż³ĢÖŠµÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£¬ÓÉ“ĖæÉÅŠ¶Ļ£Ø £©
C(g)£«D(g)¹ż³ĢÖŠµÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£¬ÓÉ“ĖæÉÅŠ¶Ļ£Ø £©
| A£®1molAÓė1molB³ä·Ö·“Ó¦ŗó£¬ÄÜĮæ±ä»ÆĪŖ¦¤E |
| B£®¼ÓČė“߻ƼĮŗ󣬷“Ó¦¼Óæģ£¬¦¤E¼õŠ” |
| C£®·“Ó¦ĪļµÄ×ܼüÄÜŠ”ÓŚÉś³ÉĪļµÄ×ܼüÄÜ |
| D£®·“Ó¦“ļµ½Ę½ŗāŹ±£¬ÉżøßĪĀ¶Č£¬AµÄ×Ŗ»ÆĀŹŌö“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
°×Į×»į¶ŌČĖĢåŌģ³ÉŃĻÖŲµÄÉÕÉĖ£¬°×Į×(P4)·Ö×Ó½į¹¹ĪŖ ”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
| A£®°×Į××Å»šµćµĶ£¬ŌŚæÕĘųÖŠæÉ×ŌČ¼ |
| B£®°×Į×”¢ŗģĮ×»„ĪŖĶ¬ĖŲŅģŠĪĢå |
| C£®31 g°×Į×ÖŠ£¬ŗ¬P”ŖP¼ü1£®5 mol |
| D£®ŅŃÖŖP4(°×Į×£¬s)£«3O2(g)===2P2O3(s)””¦¤H£½£Q kJ”¤mol£1£¬Ōņ°×Į×µÄČ¼ÉÕČČĪŖQ kJ”¤mol£1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ŅŃÖŖĒāĘųŌŚĀČĘųÖŠČ¼ÉÕŹ±²śÉś²Ō°×É«»šŃę£¬ŌŚ·“Ó¦¹ż³ĢÖŠ£¬ĘĘ»µ1 molĒāĘųµÄ»Æѧ¼üĻūŗĵÄÄÜĮæĪŖQ1 kJ£¬ĘĘ»µ1 molĀČĘųµÄ»Æѧ¼üĻūŗĵÄÄÜĮæĪŖQ2kJ £¬ŠĪ³É1 molĀČ»ÆĒāÖŠµÄ»Æѧ¼üĻūŗĵÄÄÜĮæĪŖQ3kJ£¬ĻĀĮŠ¹ŲĻµŹ½ÕżČ·µÄŹĒ £Ø £©
| A£®Q1 + Q2 > Q3 | B£®Q1 + Q2 > 2Q3 | C£®Q1 + Q2 < Q3 | D£®Q1+ Q2 < 2Q3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
øł¾ŻĻĀĆęŠÅĻ¢£¬ÅŠ¶ĻĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ £Ø £©
| A£®1molH2ŗĶ0.5molO2Ėł¾ßÓŠµÄ×ÜÄÜĮæµĶÓŚ1molĘųĢ¬H2OĖł¾ßÓŠµÄ×ÜÄÜĮæ |
| B£®ĒāĘųøśŃõĘų·“Ӧɜ³ÉĖ®µÄĶ¬Ź±ĪüŹÕÄÜĮæ |
| C£®1molH2øś1/2molO2·“Ӧɜ³É1molH2O(l)ŹĶ·ÅÄÜĮæŅ»¶ØŹĒ245kJ |
| D£®2molH2(g)øś1molO2(g)·“Ӧɜ³É2molH2O(g)ŹĶ·ÅÄÜĮæ490kJ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ÕÓĘųŹĒŅ»ÖÖÄÜŌ“£¬ĖüµÄÖ÷ŅŖ³É·ÖŹĒCH4”£0£®5molCH4ĶźČ«Č¼ÉÕÉś³ÉCO2ŗĶŅŗĢ¬Ė®Ź±·Å³ö445kJµÄČČĮ棬ŌņĻĀĮŠČČ»Æѧ·½³ĢŹ½ÖŠÕżČ·µÄŹĒ
| A£®2CH4(g) + 4O2(g) =2CO2(g) + 4H2O(l) ¦¤H£½£«890kJ”¤mol£1 |
| B£®CH4(g) + 2O2(g) =CO2(g) + 2H2O(l) ¦¤H£½£«890kJ”¤mol£1 |
| C£®CH4(g) + 2O2(g) =CO2(g) + 2H2O(l) ¦¤H£½£890kJ”¤mol£1 |
| D£®1/2CH4(g) + O2(g) =1/2CO2(g) + H2O(l) ¦¤H£½£890kJ”¤mol£1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠĶĘĀŪÕżČ·µÄŹĒ£ŗ
| A£®S(g)+O2(g)==SO2(g)”÷H1£»S(s)+O2(g)==SO2(g) ”÷H2£¬Ōņ£ŗ”÷H1>”÷H2 |
| B£®C(ŹÆÄ«£¬s)=C(½šøÕŹÆ£¬S)”÷H="+1.9" kJ/mol£¬ŌņÓÉŹÆÄ«ÖĘČ”½šøÕŹÆµÄ·“Ó¦ŹĒĪüČČ·“Ó¦£¬½šøÕŹÆ±ČŹÆÄ«ĪČ¶Ø |
| C£®NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(I)”÷H=©57.4 kJ/mol£¬Ōņ£ŗŗ¬20 gNaOHµÄĻ”ČÜŅŗÓėĻ”ŃĪĖįĶźČ«·“Ó¦£¬·Å³öµÄČČĮæĪŖ28.7 kJ |
| D£®2C(s)+O2(g)=2CO(g)”÷H=©221 kJ/mol£¬ŌņĢ¼µÄČ¼ÉÕČȵČÓŚ110.5kJ/mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
¹ŲÓŚĻĀĮŠø÷Ķ¼µÄŠšŹöÖŠ²»ÕżČ·µÄŹĒ
| A£®ŅŃÖŖCOµÄČ¼ÉÕČČĪŖ283 kJ/mol,2H2(g)£«O2(g)===2H2O(g)””¦¤H£½£483.6 kJ/mol£¬ŌņĶ¼¼×±ķŹ¾COŗĶH2O(g)Éś³ÉCO2ŗĶH2µÄÄÜĮæ±ä»Æ |
| B£®Ä³ĪĀ¶ČĻĀ£¬pH£½11µÄNH3”¤H2OŗĶpH£½1µÄŃĪĖįµČĢå»ż»ģŗĻŗó(²»æ¼ĀĒ»ģŗĻŗóČÜŅŗĢå»żµÄ±ä»Æ)Ē”ŗĆĶźČ«·“Ó¦£¬·“Ó¦ŗóµÄČÜŅŗÖŠNH4+ ”¢NH3”¤H2OÓėNH3ČżÖÖĪ¢Į£µÄĘ½ŗāÅضČÖ®ŗĶĪŖ0.05 mol”¤L£1 |
| C£®ŌŚ³£ĪĀĻĀ£¬X2(g)ŗĶH2·“Ӧɜ³ÉHXµÄĘ½ŗā³£ŹżČē±ķĖłŹ¾£¬½öŅĄ¾ŻKµÄ±ä»Æ£¬¾ĶæÉŅŌĖµĆ÷ŌŚĻąĶ¬Ģõ¼žĻĀ£¬Ę½ŗāŹ±X2(“ÓF2µ½I2)µÄ×Ŗ»ÆĀŹÖš½„½µµĶ£¬ĒŅX2ÓėH2·“Ó¦µÄ¾ēĮŅ³Ģ¶ČÖš½„¼õČõ |
D£®Ķ¼ŅŅÖŠĒśĻß±ķŹ¾³£ĪĀĻĀĻņČõĖįHAµÄĻ”ČÜŅŗÖŠ¼ÓĖ®Ļ”ŹĶ¹ż³ĢÖŠ£¬ µÄ±ä»ÆĒéæö µÄ±ä»ÆĒéæö |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
¹ŲÓŚĻĀĮŠø÷Ķ¼µÄŠšŹö£¬ÕżČ·µÄŹĒ
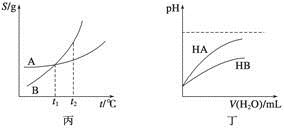
A£®¼×±ķŹ¾H2ÓėO2·¢Éś·“Ó¦¹ż³ĢÖŠµÄÄÜĮæ±ä»Æ£¬ŌņH2µÄČ¼ÉÕČČĪŖ483.6 kJ”¤mol£1
B£®ŅŅ±ķŹ¾ŗćĪĀŗćČŻĢõ¼žĻĀ·¢ÉśµÄæÉÄę·“Ó¦2NO2(g)  N2O4(g)ÖŠ£¬ø÷ĪļÖŹµÄÅضČÓėĘäĻūŗÄĖŁĀŹÖ®¼äµÄ¹ŲĻµ£¬ĘäÖŠ½»µćA¶ŌÓ¦µÄדĢ¬ĪŖ»ÆŃ§Ę½ŗāדĢ¬
N2O4(g)ÖŠ£¬ø÷ĪļÖŹµÄÅضČÓėĘäĻūŗÄĖŁĀŹÖ®¼äµÄ¹ŲĻµ£¬ĘäÖŠ½»µćA¶ŌÓ¦µÄדĢ¬ĪŖ»ÆŃ§Ę½ŗāדĢ¬
C£®±ū±ķŹ¾A”¢BĮ½ĪļÖŹµÄČܽā¶ČĖęĪĀ¶Č±ä»ÆĒéæö£¬½«A”¢B±„ŗĶČÜŅŗ·Ö±šÓÉt1”ęÉżĪĀÖĮt2”ꏱ£¬ČÜÖŹµÄÖŹĮæ·ÖŹżB£¾A
D£®¶”±ķŹ¾³£ĪĀĻĀ£¬Ļ”ŹĶHA”¢HBĮ½ÖÖĖįµÄĻ”ČÜŅŗŹ±£¬ČÜŅŗµÄpHĖę¼ÓĖ®ĮæµÄ±ä»Æ£¬ŌņĶ¬ÅØ¶ČµÄNaAČÜŅŗµÄpHŠ”ÓŚNaBČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com