
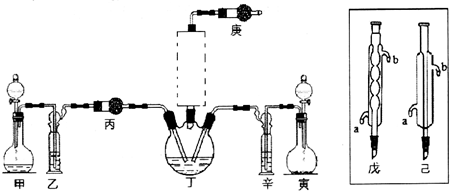
分析 制备的二氧化硫中含有水蒸气,制备的氯气中含有HCl、水蒸气,SO2C12遇水剧烈反应,需要进行干燥与除杂,甲中制备氯气,寅装置制备二氧化硫,乙为除去氯气中HCl,盛放饱和食盐水,丙干燥氯气,可以盛放为氯化钙,辛干燥二氧化硫,可以盛放浓硫酸,庚防止空气中水蒸气进入丁中,丙进行尾气处理,可以盛放碱石灰.
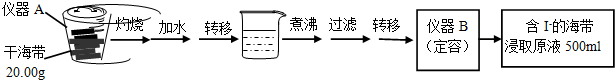
(1)①由仪器戊的结构特征,可知戊为球形冷凝管;球形冷凝管冷凝面积较直形冷凝管大,冷凝效率稍高;
②反应放热,降低温度有利于平衡正向移动;
③a.制备气体需要检查装置的气密性
b.制备的二氧化硫中含有水蒸气,制备的氯气中含有HCl、水蒸气;
c.丙中药品干燥氯气,庚中样品可以吸收水蒸气,吸收氯气与二氧化硫;
d.甲装置中制备氯气,反应不需要加热,寅装置中制备SO2;
(2)SO2Cl2常温下比较稳定,受热易分解,减压蒸馏可以降低其沸点,防止分解;
(3)根据SO2Cl2~H2SO4~BaSO4计算;
(4)SO2Cl2久置后分解会生成氯气,可能是溶解氯气所致.
解答 解:制备的二氧化硫中含有水蒸气,制备的氯气中含有HCl、水蒸气,SO2C12遇水剧烈反应,需要进行干燥与除杂,甲中制备氯气,寅装置制备二氧化硫,乙为除去氯气中HCl,盛放饱和食盐水,丙干燥氯气,可以盛放为氯化钙,辛干燥二氧化硫,可以盛放浓硫酸,庚防止空气中水蒸气进入丁中,丙进行尾气处理,可以盛放碱石灰.
(1)①由仪器戊的结构特征,可知戊为球形冷凝管;球形冷凝管冷凝面积较直形冷凝管大,冷凝效率稍高,故虚框中未画出的仪器最好选用戊,
故答案为:球形冷凝管;戊;
②该反应为反应放热,降低温度使平衡正向移动,有利于二氯化砜的生成,
故答案为:该反应为反应放热,降低温度使平衡正向移动,有利于二氯化砜的生成;
③a.制备气体装置气密性要好,组装仪器后首先要进行的操作是检查装置的气密性,故a正确;
b.甲中制备氯气,寅装置制备二氧化硫,乙为除去氯气中HCl,丙干燥氯气,辛干燥二氧化硫,故b正确;
c.丙中药品干燥氯气,庚中样品可以吸收水蒸气,吸收氯气与二氧化硫,两装置中药品不能相同,故c错误;
d.甲装置中制备氯气,反应不需要加热,可用KMnO4和浓盐酸反应制C12,寅装置中制备SO2,可用浓硫酸和Na2SO3反应制SO2,故d正确,
故选:c;
(2)SO2Cl2常温下比较稳定,受热易分解,减压蒸馏可以降低其沸点,防止分解,
故答案为:降低二氯化砜的沸点,减少二氯化砜的分解;
(3)设所得馏分中二氯化砜的质量百分含量为x,则:
SO2Cl2~H2SO4~BaSO4
135 233
1.00g×x 1.6g
所以135:233=1.00g×x:1.6g
解得x=92.7%
故答案为:92.7;
(4)SO2Cl2久置后分解会生成氯气,可能是溶解氯气所致,
故答案为:二氯化砜久置后分解会生成氯气的溶解再二氯化砜中.
点评 本题考查物质制备实验,涉及对反应原理、装置及操作的分析评价、对仪器的识别、物质的分离提纯等,注意对物质性质信息的应用,难度中等.


 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:解答题
| V(AgNO3)/mL | 15.00 | 19.00 | 19.80 | 19.98 | 20.00 | 20.02 | 21.00 | 23.00 | 25.00 |
| E/mV | -225 | -200 | -150 | -100 | 50.0 | 175 | 275 | 300 | 325 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O $\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3↓+3H+ | |
| B. | 酸性KI淀粉溶液久置后变蓝 4I-+O2+2H2O═2I2+4OH- | |
| C. | 实验室盛装NaOH溶液的试剂瓶不能用玻璃塞SiO2+2OH-═SiO32-+H2O | |
| D. | 向次氯酸钙溶液通入SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质氧化性的强弱 | |
| B. | 最高价氧化物对应的水化物酸性的强弱 | |
| C. | 单质沸点的高低 | |
| D. | 单质与氢气化合的难易 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
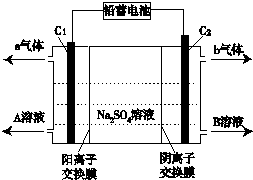
| A. | C1极电极与铅蓄电池的Pb电极相接,C2极与铅蓄电池的PbO2电极相接 | |
| B. | 当C1极产生标准状况下11.2 L气体时,铅蓄电池的负极增重64g | |
| C. | A溶液为氢氧化钠溶液,B溶液为硫酸 | |
| D. | 该电解反应的总方程式可以表示为:2Na2SO4+6H2O$\frac{\underline{\;电解\;}}{\;}$2H2SO4+4NaOH+O2↑+2H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
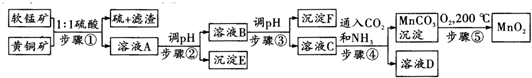
| 沉淀物 | Cu(OH)2 | Fe(OH)3 | Mn(OH)2 | Fe(OH)2 |
| 开始沉淀pH | 4.2 | 1.5 | 7.3 | 6.4 |
| 完全沉淀pH | 6.7 | 3.2 | 9.8 | 9.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | l mol H20最多可形成氢键数目为2NA | |
| B. | 标准状况下,11.2 L甲醛所含的σ键数目为2NA | |
| C. | 常温下,46 g N02所含分子数目为NA | |
| D. | pH=l的硫酸中所含S042-的数目为0.05NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com