
| A. | 硅酸钠溶液中通入CO2气体:SiO32-+H2O+CO2═H2SiO3↓+CO32- | |
| B. | 氯气与氢氧化钾溶液反应:Cl2+OH-═Cl-+ClO-+2H2O | |
| C. | 硫酸铝与氨水反应:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 小苏打溶液与稀盐酸反应:HCO3-+H+═H2O+CO2↑ |
分析 A.硅酸钠溶液与二氧化碳反应生成硅酸沉淀和碳酸钠;
B.离子方程式两边负电荷不相等,违反了电荷守恒;
C.硫酸铝与氨水反应生成氢氧化铝沉淀和硫酸铵;
D.小苏打为碳酸氢钠,碳酸氢钠与稀盐酸反应生成氯化钠、二氧化碳气体和水.
解答 解:A.硅酸钠溶液中通入CO2气体,二者反应生成硅酸和碳酸钠,反应的离子方程式为:SiO32-+H2O+CO2═H2SiO3↓+CO32-,故A正确;
B.氯气与氢氧化钾溶液反应生成氯化钾、次氯酸钾和水,正确的离子方程式为:Cl2+2OH-═Cl-+ClO-+2H2O,故B错误;
C.硫酸铝与氨水反应生成硫酸铵和氢氧化铝沉淀,反应的离子方程式为:Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故C正确;
D.小苏打溶液与稀盐酸反应生成NaCl、二氧化碳和水,反应的离子方程式为:HCO3-+H+═H2O+CO2↑,故D正确;
故选B.
点评 本题考查了离子方程式的书写判断,为高考的高频题,题目难度不大,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


科目:高中化学 来源: 题型:选择题
| 选项 | 实验现象 | 原因分析 |
| A | 久置的浓硝酸呈黄色 | 浓硝酸不稳定,分解生成的NO2 溶解在其中 |
| B | 铝片先用砂纸打磨,再加入到浓硝酸中,无明显现象 | 浓硝酸具有强氧化性,常温下,铝被浓硝酸钝化 |
| C | SO2通入酸性高锰酸钾溶液中,溶液紫红色褪去 | SO2具有漂白性,使其褪色 |
| D | 向湿润蔗糖中加入浓硫酸,固体迅速变黑,后体积急剧膨胀 | 在浓硫酸脱水作用下,蔗糖被炭化,炭与浓硫酸反应生成了CO2、SO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
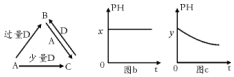
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1的醋酸加水稀释,$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$减小 | |
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw变大 | |
| C. | 体积、pH均相同的醋酸和盐酸完全溶解等量的镁粉(少量)后者用时少 | |
| D. | 常温下,pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合,溶液显碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
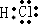 ,X2Y的结构式
,X2Y的结构式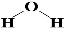 .
.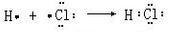 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
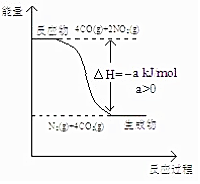 研究 NOx、SO2、CO 等大气污染气体的处理具有重要意义.
研究 NOx、SO2、CO 等大气污染气体的处理具有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在提纯鸡蛋中的蛋白质时,可向鸡蛋清溶液中加入浓硝酸,然后将所得沉淀滤出,即得较纯的蛋白质 | |
| B. | 可用过滤的方法除去四氯化碳中的I2 | |
| C. | 苯和溴苯的混合物可用分液漏斗分液分离 | |
| D. | 乙酸乙酯中混有乙酸,可用饱和Na2CO3溶液洗涤,然后分液分离出乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验编号 | 滴入NaOH(aq)的体积/mL | 溶液的pH | |
| HX | HY | ||
| ① | 0 | 3 | m |
| ② | 10.00 | x | y |
| ③ | 20.00 | n | 7 |
| A. | 相同温度下.同浓度的两种酸溶液的导电能力:HX<HY | |
| B. | 表中x<7 | |
| C. | HX和HY的混合溶液中存在:c(H+)=c(X-)+c(Y-)+c(OH-) | |
| D. | 实验②NaOH与HY反应后的溶液中:c(Na+)>c(Y-)>c(OH-)>c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com