
������������ȷ����
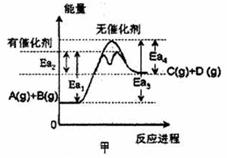

A���ɼ�֪��A��B���д������ڵ��Ȼ�ѧ����ʽΪ�� 
B�����³�ѹ�£���a mol CO2����ͨ��1L bmol/L��NaOH��Һ�У���a��2bʱ������CO2�����ͨ�룬��Һ����ˮ�������c��H��������ͼ�ұ仯��ϵ����1/2��a/b��1ʱ��������Һ��һ�����ڣ� c��Na������c��CO32-����c��HCO3������c��H2CO3��
C�������£���ϡNaOH��Һ��CH3COOH��Һ��ϣ������ܳ���pH��7��
��c��OH-����c��Na+����c��H+����c��CH3COO-�������
D��ij�¶��£�pH=11��NH3��H2O��pH=1������������Ϻ����ǻ�Ϻ���Һ����ı仯��ǡ����ȫ��Ӧ����Ӧ�����Һ��NH4+��NH3��H2O��NH3��������ƽ��Ũ��֮��Ϊ0.05mol��L-1
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ���¶��½�3 mol CO2��2 mol H2�����2 L���ܱ������У��������·�Ӧ��CO2(g)��H2(g) CO(g)��H2O(g)
CO(g)��H2O(g)
(1)�÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽK��__________��
(2)��֪��700��ʱ���÷�Ӧ��ƽ�ⳣ��K1��0.6������¶��·�ӦCO(g)��H2O(g) CO2(g)��H2(g)��ƽ�ⳣ��K2��__________��
CO2(g)��H2(g)��ƽ�ⳣ��K2��__________��
(3)��֪��1000��ʱ���÷�Ӧ��ƽ�ⳣ��K3Ϊ1.0����÷�ӦΪ__________��Ӧ(����ȡ����ȡ�)��
(4)���жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������__________________��
A��������ѹǿ���� B��c(CO2)��c(CO) C������a mol CO2��ͬʱ����a mol H2 D����������ƽ����Է�����������
(5)��1000���£�ijʱ��CO2�����ʵ���Ϊ2.0 mol�����ʱv(��)______v(��)
(�>������������<��)�����¶��·�Ӧ�ﵽƽ��ʱ��CO2��ת����Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������һ�������£����Ƶýϴ�����1,2������������ǣ� ��
A ��������������� B����ϩ���Ȼ�����
C����ϩ��������� D����Ȳ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����κ�һ����ѧƽ����ϵ�����±仯���ȡ�Ĵ�ʩ��ʹƽ��һ�������ƶ����ǣ�
�ټ���һ�ַ�Ӧ�� ��������ϵ��ѹǿ �������¶� ��ʹ�ô��� �ݻ�ѧƽ�ⳣ����С
A���٢ڢۢ� B���٢ڢۢܢ� C���ۢ� D���٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ö��Ե缫���һ��Ũ�ȵ�����ͭ��Һ��ͨ��һ��ʱ��������õ���Һ�м���0.1mol Cu2��OH��2CO3�����ǡ�ûָ������ǰ��Ũ�Ⱥ�pHֵ�������Ƕ�����̼���ܽ⣩����������й�ת�Ƶĵ������ʵ���Ϊ
A.0.4mol B.0.5mol C.0.6mol D.0.8mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������һЩ���ʵ��۷е����ݣ���ѹ����
| �� | �� | Na2CO3 | ���ʯ | ʯī | |
| �۵㣨�棩 | 63.65 | 97.8 | 851 | 3550 | 3850 |
| �е㣨�棩 | 774 | 882.9 | 1850���ֽ����CO2�� | ---- | 4250 |
�����ƺ�CO2�ڳ�ѹ��890�淢�����·�Ӧ��
4 Na��g��+ 3CO2��g��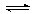 2 Na2CO3��l�� + C(s,���ʯ) ��H=��1080.9kJ/mol
2 Na2CO3��l�� + C(s,���ʯ) ��H=��1080.9kJ/mol
��1��������Ӧ��ƽ�ⳣ������ʽΪ ��
��4v��(Na)= 3v��(CO2)����Ӧ�Ƿ�ﵽƽ�� ��ѡ��ǡ�����
��2����CO2��g��+4Na��g��=2Na2O��s��+C��s�����ʯ�� ��H=��357.5kJ/mol����Na2O������C�����ʯ����Ӧ�õ�Na��g����Һ̬Na2CO3��l�����Ȼ�ѧ����ʽ ��
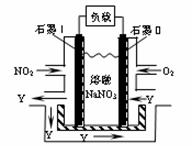
(3)NO2��O2������NaNO3������ȼ�ϵ�أ���ԭ����ͼ���õ����ʹ�ù�����ʯīI�缫������������Y����缫��ӦΪ:
������1molY������Ҫ���ı�״������������
��Ϊ L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��B��CΪ���ֶ�����Ԫ��A��B��ͬ���ڣ�A��C����ͼ����ӷֱ�ΪA2����C����B2����C��������ͬ�ĵ��Ӳ�ṹ������˵������ȷ���� �� ��
A��ԭ��������C>A��B B�����Ӱ뾶��A2����C����B2��
C��ԭ�Ӱ뾶��A��B��C D��ԭ�Ӻ���������������A��C��B
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
25��ʱ����һ���Ϊ2L���ܱ������У���̬����A��B��C�����ʵ���n(mol)��ʱ��t�ı仯����ͼ��ʾ����֪��ƽ������¶ȣ�A��ת��������

(1)������ͼ���ݣ��ӷ�Ӧ��ʼ�����һ��ƽ��ʱ��ƽ������v(A)Ϊ ��
(2)��25��ʱ���ﵽ��һ��ƽ�⣬��˷�Ӧ�ķ���ʽΪ ��
(3)��5~7min�ڣ����¶Ȳ��䣬��˴����߱仯��ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Ϊͬ���칹������ʲ����ܾ���
A����ͬ��ʽ�� B����ͬ�Ľṹ C����ͬ��ͨʽ D����ͬ�ķ���ʽ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com