
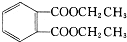 )是一种重要的工业塑化剂,其合成路线很多,下图就是其中的一种合成方法:
)是一种重要的工业塑化剂,其合成路线很多,下图就是其中的一种合成方法: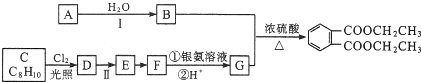
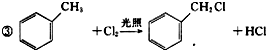
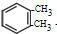 +2Cl2$\stackrel{光照}{→}$
+2Cl2$\stackrel{光照}{→}$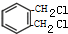 +2HCl.
+2HCl. .
.分析 由邻苯二甲酸二乙酯结构可知,邻苯二甲酸和乙醇发生酯化反应生成,有机化合物A可用来催熟水果,A为CH2=CH2,CH2=CH2中含有不饱和的C=C双键,能够在催化剂存在条件下与水发生加成反应生成B为CH3CH2OH;
G为邻苯二甲酸 ,含几种位置的H原子,则核磁共振氢谱就有几种,有机化合物C化学式为C8H10,核磁共振氢谱显示有3种不同化学环境的氢原子,说明含有3种氢原子,则C为
,含几种位置的H原子,则核磁共振氢谱就有几种,有机化合物C化学式为C8H10,核磁共振氢谱显示有3种不同化学环境的氢原子,说明含有3种氢原子,则C为 ,与氯气发生取代反应生成D为
,与氯气发生取代反应生成D为 ,F能发生银镜反应,说明F为醛,且G为邻苯二甲酸,所以F
,F能发生银镜反应,说明F为醛,且G为邻苯二甲酸,所以F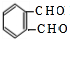 ,则E→F为醇的催化氧化,所以E为
,则E→F为醇的催化氧化,所以E为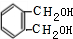 ,D→E为卤代烃的取代反应,据此分析解答.
,D→E为卤代烃的取代反应,据此分析解答.
解答 解:由邻苯二甲酸二乙酯结构可知,邻苯二甲酸和乙醇发生酯化反应生成,有机化合物A可用来催熟水果,A为CH2=CH2,CH2=CH2中含有不饱和的C=C双键,能够在催化剂存在条件下与水发生加成反应生成B为CH3CH2OH;
G为邻苯二甲酸 ,含几种位置的H原子,则核磁共振氢谱就有几种,有机化合物C化学式为C8H10,核磁共振氢谱显示有3种不同化学环境的氢原子,说明含有3种氢原子,则C为
,含几种位置的H原子,则核磁共振氢谱就有几种,有机化合物C化学式为C8H10,核磁共振氢谱显示有3种不同化学环境的氢原子,说明含有3种氢原子,则C为 ,与氯气发生取代反应生成D为
,与氯气发生取代反应生成D为 ,F能发生银镜反应,说明F为醛,且G为邻苯二甲酸,所以F
,F能发生银镜反应,说明F为醛,且G为邻苯二甲酸,所以F ,则E→F为醇的催化氧化,所以E为
,则E→F为醇的催化氧化,所以E为 ,D→E为卤代烃的取代反应,
,D→E为卤代烃的取代反应,
(1)A的化学名称是乙烯,B为乙醇,结构简式为CH3CH2OH,故答案为:乙烯;CH3CH2OH;
(2)反应II为卤代烃的水解反应,其反应条件是强碱的水溶液、加热,所以所用试剂是强碱水溶液,该反应为取代反应或水解反应,故答案为:强碱的水溶液;取代(或水解);
(3)有机化合物C化学式为C8H10,核磁共振氢谱显示有3种不同化学环境的氢原子,说明含有3种氢原子,则C为 ,与氯气发生取代反应
,与氯气发生取代反应 +2Cl2$\stackrel{光照}{→}$
+2Cl2$\stackrel{光照}{→}$ +2HCl,
+2HCl,
故答案为: +2Cl2$\stackrel{光照}{→}$
+2Cl2$\stackrel{光照}{→}$ +2HCl;
+2HCl;
(4)E生成F为醇的催化氧化,反应方程式为 ,故答案为:
,故答案为: ;
;
(5)G为邻苯二甲酸 ,满足下列条件的同分异构体:
,满足下列条件的同分异构体:
能与新制的Cu(OH)2 悬浊液混合加热生成砖红色沉淀,含有醛基,又能与碳酸钠反应生成二氧化碳,含有羧基,能与FeCl3 溶液发生显色反应,含有酚羟基;说明苯环上有-OH、-CHO、-COOH三个取代基,-OH、-CHO处于邻位,-COOH有4种位置,-OH、-CHO处于间位,-COOH有4种位置,-OH、-CHO处于对位,-COOH有2种位置,有10种;所有这些同分异构体中,不同化学环境氢原子的种数都为6种,
故答案为:10;相同.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析判断及知识综合应用能力,根据某些物质结构简式结合反应条件、题给信息进行推断,难点是同分异构体种类判断,要考虑位置异构、碳链异构,题目难度中等.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.46g | B. | 0.69g | C. | 0.92g | D. | 0.23g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 均为0.56 L | B. | ①=② | C. | ①>② | D. | ②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
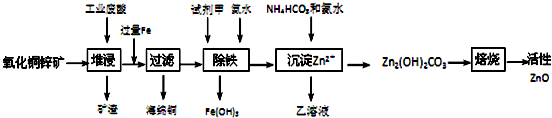
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
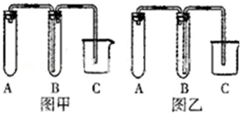 化学是一门以实验为基础的学科.
化学是一门以实验为基础的学科.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能使甲基橙变红的溶液中:Fe2+、Al3+、NO3-、Cl-、S2- | |
| B. | 在pH=11的溶液中:Na+、AlO2-、NO3-、S2-、SO32- | |
| C. | 室温下,由水电离的c(H+)=10-10mol/L的溶液中:Cl-、HCO3-、NO3-、NH4+、F- | |
| D. | 0.1 mol•L-1 FeCl3溶液中:K+、Na+、AlO2-、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 离子组 | 评 价 |
| A | H+、Fe2+、NO3-、Cl- | 不能大量共存于同一溶液中,因为发生了氧化还原反应: 4Fe2++2NO3-+6H+═4Fe3++2NO↑+3H2O |
| B | Na+、CO32-、Cl-、Al3+ | 不能大量共存于同一溶液中,因Al3+和CO32-都要发生水解且相互促进:2Al3++3CO32-+3H2O═2Al(OH)3↓+3CO2↑ |
| C | Fe3+、K+、SCN-、Br- | 不能大量共存于同一溶液中,因为有红色沉淀生成: Fe3++3SCN-═Fe(SCN)3↓ |
| D | HCO3-、OH-、Na+、Ca2+ | 不能大量共存于同一溶液中,因会发生如下反应: HCO3-+OH-═CO2↑+H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com