
【题目】某化学教师为“氯气与金属钠反应”设计了如图装置与操作以替代相关的课本实验。玻璃管内放一块黄豆粒大的金属钠(已吸净煤油),玻璃管尾部塞一团浸有NaOH溶液的棉花球。先给钠预热,待钠熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。以下叙述错误的是( )

A. 反应生成的大量白烟是氯化钠晶体
B. 浸有NaOH溶液的棉花球用于吸收过量的氯气,以免其污染空气
C. 钠着火燃烧产生苍白色火焰
D. 在棉花球外沿滴一滴石蕊溶液,判断氯气是否被碱液完全吸收
科目:高中化学 来源: 题型:
【题目】居民所用石油液化气的主要成分是丁烷,在使用过程中,常有一些杂质以液态沉积于钢瓶中,这些杂质可能是( )
A. 甲烷和丙烷 B. 丁烷和甲醛 C. 乙烷和丁烷 D. 戊烷和己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中错误的是( )
A.只要是糖类物质都能与银氨溶液发生银镜反应B.单糖是不能发生水解的最简单的糖类
C.淀粉、纤维素都是天然有机高分子化合物D.蔗糖和麦芽糖均为二糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在托盘天平的两盘,放上质量相等的A、B两烧杯,调至平衡,然后分别倒入质量相等的足量盐酸,继而在AB两烧杯中放入下述各组物质,结果天平仍保持平衡的是()
A. 0.5molNa和0.5molMg B. 0.1molZn和0.1molAl
C. 8.4gMgCO3和8.4gNaHCO3 D. 10gCaCO3和10gMgCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为常见温室气体,B为淡黄色氧化物,C为常见液体,D为黄绿色气体单质,相互反应的关系如右图所示,M的水溶液能杀菌消毒。下列有关叙述正确的是
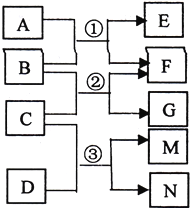
A. 4.4gA含有4.4NA个质子
B. 7.8gB与足量A发生反应①,共转移0.2NA电子
C. 反应③的离子方程式为:Cl2+H2O![]() 2H++Cl-+ ClO-
2H++Cl-+ ClO-
D. M的电子式为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中,除了22种非金属元素外,其余的都是金属,请根据元素周期表回答下列问题:
I.(1)基态氮原子核外共有_______种运动状态不相同的电子,该原子核外电子排布中电子在能量最低的轨道呈_______形,用n表示能层,氟元素所在族的外围电子排布式为______________。
(2)在元素周期表中,某些主族元素与下方的主族元素的性质有些相似,被称为“对角线规则”,如下表:

根据“对角线规则”写出Be(OH)2与NaOH反应的离子方程式______________,硼酸(H3BO3)是一种具有片层结构的白色晶体,层内的H3BO3分子间通过氢键相连(如图)。含1mol H3BO3的晶体中有__________mol氢键,H3BO3中B原子的杂化类型为_____________。

(3)以第二周期为例,除Be、N外,其它元素的第一电离能从左到右逐渐增大的原因是____________________________________________________。
II.近年来铁及其化合物在工农业中有广阔的应用前景。
(4)铁的一种络离子[Fe(CN)6]4-中Fe2+的配位数为6,该络离子中不存在______(填序号)。
A.共价键 B.非极性键 C.配位键 D.δ键 E.π键
(5)AlCl3的熔点比NaCl熔点低的原因是____________________________________。
(6)一种Al-Fe合金的立体晶胞如图所示。若晶体的密度为ρ gcm-3,则此合金中最近的两个Fe原子之间的距离为__________cm(用含ρ的代数式表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物的合成路线中,已知:
①A为烃类化合物,质谱图表明其相对分子质量为92,红外光谱表明分子中没有碳碳双键,核磁共振氢谱显示A有4组峰,其峰面积之比为3∶2∶2∶1
②E是一种烃,对H2的相对密度为14,所有原子均在一个平面内。
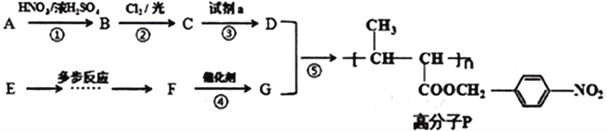
根据以上合成路线回答下列问题:
(1)A物质的名称____________________,步骤③中的试剂a及条件是_______________________。
(2)反应②的化学方程式是________________________________。
(3)F的分子式是C4H6O2,F中含有的官能团名称是__________________________________。
(4)反应①的类型__________________________________。
(5)反应⑤的化学方程式是__________________________________。
(6)与D具有相同的分子式,含硝基(—NO2)且苯环上有两个取代基的同分异构体还有________种(D除外)。
(7)已知:![]() ,以E为起始原料,选用必要的无机试剂合成F,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂与反应条件)______。
,以E为起始原料,选用必要的无机试剂合成F,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂与反应条件)______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用氯化铜晶体(CuCl2·2H2O,含氯化亚铁杂质)制取纯净的CuCl2·2H2O。先将其制成水溶液,后按如图步骤进行提纯:

已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见下表
金属离子 | Fe3+ | Fe2+ | Cu2+ |
氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
氢氧化物沉淀完全时的pH | 3.2 | 9.0 | 6.7 |
请回答下列问题:
(1)现有氧化剂NaClO、H2O2、KMnO4,X加哪种好,为什么?________________________________,该反应的离子方程式为_________________________________。
(2)溶液II中除Cu2+外,还有______金属离子,检验试剂为______________。物质Y不能为下列的________________________。
a.CuO b.Cu(OH)2 c.CuCO3 d.Cu2(OH)2CO3 e.CaO f.NaOH
(3)常温下,除去CuCl2溶液中的Fe2+,加入氧化剂X,使Fe2+氧化为Fe3+,然后加入物质Y至溶液pH=4,此时c(Fe3+)=_________mol/L,[已知Fe(OH)3的Ksp=4×10-38]
(4)若在空气中加热固体CuCl2·2H2O,可水解生成Cu(OH)Cl,写出相关的化学方程式_______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com