
| A. | 124g P4含有的P-P键数为4NA(设NA表示阿伏伽德罗常数的值) | |
| B. | Be和NaOH溶液反应的离子方程式是:2Be+2OH -+2H2O=2BeO2-+3H2↑ | |
| C. | 在NaCl溶液中加入AgNO3溶液,生成白色沉淀;再加入氨水,沉淀消失,沉淀消失发生的离子方程式是: AgCl+2NH3•H2O=[Ag(NH3)2]++Cl-+2H2O | |
| D. | 0.1mol/L的Fe3+溶液中,能大量共存的离子有Cl-、SO42-、SCN- |
分析 A.n(P4)=$\frac{124g}{124g/mol}$=1mol,每个P4分子中含有6个P-P键;
B.Be的性质和Al相似,Be和NaOH溶液反应生成Na2BeO2、H2;
C.AgCl和一水合氨反应生成银氨溶液和水;
D.Fe3+、SCN-发生络合反应.
解答 解:A.n(P4)=$\frac{124g}{124g/mol}$=1mol,每个P4分子中含有6个P-P键,则1mol白磷中含有6molP-P键,所以124g P4含有的P-P键数为4NA,故A错误;
B.Be的性质和Al相似,Be和NaOH溶液反应生成Na2BeO2、H2,离子方程式为Be+2OH-=BeO22-+H2↑,故B错误;
C.AgCl和一水合氨反应生成银氨溶液和水,离子方程式为AgCl+2NH3•H2O=[Ag(NH3)2]++Cl-+2H2O,故C正确;
D.Fe3+、SCN-发生络合反应生成络合物硫氰化铁而不能大量共存,故D错误;
故选C.
点评 本题考查离子共存、离子方程式的书写、物质的量的计算等知识点,为高频考点,侧重考查学生分析、判断、知识迁移能力,明确离子性质、物质结构是解本题关键,注意:白磷分子是正四面体结构,每个顶点上含有1个P原子,题目难度不大.


 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 单质:金刚石、白磷 | B. | 酸性氧化物:SO3、CO2、NO | ||
| C. | 混合物:铝热剂、矿泉水、焦炉气 | D. | 同素异形体:C60、C70、金刚石 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,7.8gNa2S固体和7.8gNa2O2固体中含有的阴离子数目均为0.1NA | |
| B. | 在标准状况下,22.4LCl2和HCl的混合气体中含有的分子总数为2×6.02×1023 | |
| C. | 含1molFeCl3的饱和溶液滴入沸水中得到胶体数目为NA | |
| D. | 标准状况下,1molNa2O2的体积是22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴有酚酞的碳酸氢钠溶液显红色,微热后红色加深,是因为碳酸氢钠分解生成了碳酸钠 | |
| B. | 用洁净的玻璃管向包有过氧化钠的脱脂棉吹气,脱脂棉燃烧,说明二氧化碳、水与过氧化钠的反应是放热反应 | |
| C. | 向溴水中滴入植物油,振荡后油层显无色,说明溴不溶于油脂 | |
| D. | 粗锌与稀硫酸反应制氢气比纯锌快,是因为粗锌比纯锌还原性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
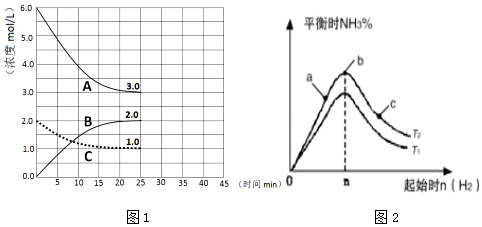
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子最外层电子数为2的元素一定处于周期表IIA族 | |
| B. | 元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 | |
| C. | 某元素原子核外的电子数为63,则它是第6周期副族元素 | |
| D. | 除短周期外,其他周期均为18种元素,副族元素没有非金属元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com