
第4周期元素由于受3d能级电子的影响,性质的递变规律与短周期元素略有不同。
Ⅰ.第4周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的。镓(31Ga)的基态原子的电子排布式是 ;31Ga的第一电离能却明显低于30Zn的,原因是
。
Ⅱ.第4周期过渡元素的明显特征是形成多种多样的配合物。
(1)CO和NH3可以和很多过渡金属形成配合物。CO与N2互为等电子体,CO分子中C原子上有一对孤电子对,C、O原子都符合8电子稳定结构,则CO的结构式可表示为 。NH3分子中N原子的杂化方式为 杂化,NH3分子的空间立体构型是 。
(2)如图甲所示为二维平面晶体示意图,所表示的化学式为AX3的是 。

(3)图乙为一个铜晶胞,此晶胞立方体的边长为a cm,Cu的相对原子质量为64,金属铜的密度为ρ g/cm3,则阿伏加德罗常数可表示为 mol-1(用含a、ρ的代数式表示)。
Ⅰ.1s22s22p63s23p63d104s24p1 30Zn的4s能级处于全充满状态,较稳定
Ⅱ.(1)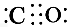 (或C
(或C O) sp3 三角锥形
O) sp3 三角锥形
(2)b (3)
【解析】Ⅰ.根据构造原理,31Ga的基态原子的电子排布式是1s22s22p63s23p63d104s24p1;因30Zn的4s能级处于全充满状态,较稳定。
Ⅱ.(1)因为“CO与N2互为等电子体”,故其具有相同的结构,由N2的结构、“C原子上有一对孤电子对”和“C、O原子都符合8电子稳定结构”可知,CO的结构式可表示为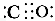 (或C
(或C O);NH3分子中中心原子N的杂化方式为sp3杂化,空间构型为三角锥形。(2)a图中1个黑球周围有6个相邻白球,1个白球周围有3个相邻黑球,故黑∶白=1∶2;b图中1个黑球周围有6个相邻白球,1个白球周围有2个相邻黑球,故黑∶白=1∶3。(3)一个铜晶胞所含有的铜原子数为
O);NH3分子中中心原子N的杂化方式为sp3杂化,空间构型为三角锥形。(2)a图中1个黑球周围有6个相邻白球,1个白球周围有3个相邻黑球,故黑∶白=1∶2;b图中1个黑球周围有6个相邻白球,1个白球周围有2个相邻黑球,故黑∶白=1∶3。(3)一个铜晶胞所含有的铜原子数为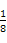 ×8+
×8+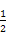 ×6=4,由ρ g/cm3=
×6=4,由ρ g/cm3=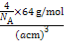 得:NA=
得:NA= mol-1。
mol-1。


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源:2014高考化学名师选择题专练 有机物组成练习卷(解析版) 题型:选择题
下列关于有机物因果关系的叙述中,完全正确的一组是( )
选项原因结论
A乙烯和苯都能使溴水褪色苯和乙烯都能与溴水发生加成反应
B乙酸分子中含有羧基可与NaHCO3溶液反应生成CO2
C纤维素和淀粉的化学式均为(C6H10O5)n它们属于同分异构体
D乙酸乙酯和乙烯在一定条件下都能与水反应两者属于同一反应类型
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 化学与STSE练习卷(解析版) 题型:选择题
化学与人类生产、生活、社会可持续发展密切相关,下列说法不正确的是( )
A.“天宫一号”中使用的碳纤维,是一种新型无机非金属材料
B.为防止中秋月饼等富脂食品氧化变质,常在包装袋中放入生石灰
C.用CO2合成聚碳酸酯可降解塑料,实现“碳”的循环利用
D.汽车排放的尾气和冬季取暖排放颗粒污染物是形成雾霾的重要因素
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 NA的应用练习卷(解析版) 题型:选择题
设阿伏加德罗常数的值为NA,下列说法正确的是( )
A.标准状况下,22.4 L一氯甲烷和二氯甲烷的混合物所含氯原子数介于NA至2NA之间。
B.1 mol的Cu在一定条件下与足量硫粉反应,转移电子数目为2NA
C.3.65 g液态氯化氢中分子的数目为0.1NA
D.常温下5.6 g铁投入足量的浓硝酸中,转移的电子数为0.3NA
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 NA的应用练习卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.0.5 mol/L MgCl2溶液中Cl-的数目为NA
B.58 g乙烯和乙烷的混合气体中碳原子数目一定为4NA
C.常温常压下,22.4 L NO和N2的混合气体中分子数目大于NA
D.标准状况下,0.5 mol氦气含有的电子数为NA
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师综合题专练 物质性质综合应用练习卷(解析版) 题型:填空题
某工业废渣的主要成分为SiO2、Fe2O3、Al2O3、MgO。现根据下列方案对其进行处理以回收废渣中的金属元素。
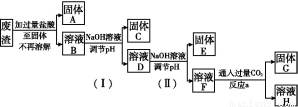
回答下列问题。
(1)固体A的化学式为 。
(2)反应a的化学反应方程式为 。
(3)25 ℃时,溶液中金属离子的物质的量浓度与溶液pH的关系如图所示:

①调节pH(Ⅰ)的pH为 ;
②溶液D加入氢氧化钠溶液的同时调节pH(Ⅱ)所发生反应的离子方程式为 ;
③从图中数据计算可得Mg(OH)2的溶度积Ksp[Mg(OH)2]约为 。
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师综合题专练 有机合成与推断练习卷(解析版) 题型:填空题
兔耳草醛是食品与化妆品工业中的香料添加剂。工业上可通过有机化工原料A制得,其合成路线如下图所示:
A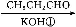 B
B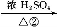 C
C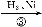 D
D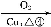
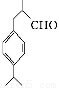 (兔耳草醛)
(兔耳草醛)
已知:①CH3CHO+CH3CHO CH3CH(OH)CH2CHO
CH3CH(OH)CH2CHO
②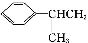 可写成
可写成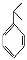
(1)B中含氧官能团的名称是 。
(2)上述合成路线中反应①属于 ,反应②属于 (填写反应类型)。
(3)写出由D获得兔耳草醛的化学反应方程式: 。
(4)A的同分异构体中符合以下条件的有 种。
a.能使FeCl3溶液显紫色
b.能发生加聚反应
c.苯环上只有两个互为对位的取代基
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师综合题专练 化学反应原理练习卷(解析版) 题型:填空题
恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图1所示。已知:2SO2(g)+O2(g) 2SO3(g)
2SO3(g)
ΔH=-196.6 kJ/mol。

请回答下列问题:
(1)写出能表示硫的燃烧热的热化学方程式: 。
(2)ΔH2= 。
(3)恒温恒容时,1 mol SO2和2 mol O2充分反应,放出热量的数值比∣ΔH2∣ (填“大”、“小”或“相等”)。
(4)将Ⅲ中的混合气体通入足量的NaOH溶液中消耗NaOH的物质的量为 ,若溶液中发生了氧化还原反应,则该过程的离子方程式为 。
(5)恒容条件下,下列措施中能使n(SO3)/ n(SO2)增大的有 。
a.升高温度
b.充入He气
c.再充入1 mol SO2(g)和1 mol O2(g)
d.使用催化剂
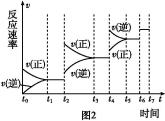
(6)某SO2(g)和O2 (g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2 (g)的量,则图中t4时引起平衡移动的条件可能是 ;图中表示平衡混合物中SO3的含量最高的一段时间是 。
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题8化学反应速率与化学平衡练习卷(解析版) 题型:选择题
用来表示可逆反应:2A(g)+B(g) 2C(g) ΔH<0 的正确图像是下图中的( )
2C(g) ΔH<0 的正确图像是下图中的( )
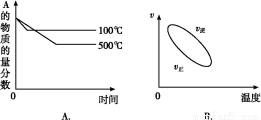

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com