

| A. | 该有机物属于芳香烃 | |
| B. | 该物质不能使酸性高锰酸钾溶液褪色 | |
| C. | 该分子对称性好,所以没有顺反异构 | |
| D. | 该有机物分子中,最多可能有18个碳原子共平面 |
分析 A.芳香烃中只含C、H元素且含有苯环;
B.含有碳碳不饱和键、醛基或连接苯环的碳原子上含有氢原子的苯的同系物能被酸性高锰酸钾溶液氧化;
C.该物质结构对称,但含有顺反异构;
D.连接碳碳双键两端的C原子共面,苯环上所有C原子共面.
解答 解:A.芳香烃中只含C、H元素且含有苯环,该物质中还含有O元素,属于烃的含氧衍生物,不属于芳香烃,故A错误;
B.含有碳碳不饱和键、醛基或连接苯环的碳原子上含有氢原子的苯的同系物能被酸性高锰酸钾溶液氧化,该物质中含有碳碳不饱和键,且连接苯环的碳原子上含有氢原子,所以能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,故B错误;
C.该物质结构对称,但碳碳两端的碳原子连接基团不同,所以含有顺反异构,故C错误;
D.连接碳碳双键两端的C原子共面,苯环上所有C原子共面,所以该有机物分子中,最多可能有18个碳原子共平面,故D正确;
故选D.
点评 本题考查有机物结构和性质、物质结构及基本概念,为高频考点,明确官能团及其性质再结合乙烯、苯结构确定共面碳原子个数,易错选项是D,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 该反应为吸热反应 | B. | CO2分子由极性键形成的极性分子 | ||
| C. | HCHO分子中有3个σ键,1个π键 | D. | 每生成1.8gH2O消耗2.24L O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
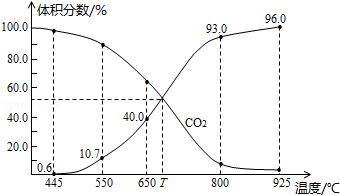
| A. | 550℃时,若充入惰性气体,v正,v逆均减小 | |
| B. | 650℃时,反应达平衡后CO2的转化率为25.0% | |
| C. | T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动 | |
| D. | 925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=23.04P总 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该硫酸试剂的物质的量浓度为18.4 mol/L | |
| B. | 稀释该硫酸时应把水倒入硫酸中,边倒边搅拌 | |
| C. | 50 mL该H2SO4中加入足量的铜片并加热,被还原的H2SO4的物质的量为0.46 mol | |
| D. | 标准状况下2.7 g Al与足量的该硫酸反应可得到H2 3.36 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 如试管外壁有水,应在加热前擦拭干净 | |
| B. | 先使试管均匀受热,即先进行预热,然后把灯焰固定在放固体的部位加热 | |
| C. | 试管夹夹在距试管口约$\frac{1}{3}$处 | |
| D. | 加热完毕,立即用冷水冲洗试管 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 32g氧气和臭氧的混合气体中所含的原子数为2NA | |
| B. | 常温常压下,22.4LCO2含有的分子数目为NA | |
| C. | 2.4g金属镁与足量的盐酸反应,转移的电子数为0.2NA | |
| D. | 0.1mol OH-含有NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
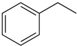 (g)→
(g)→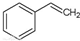 (g)+H2(g),△H=+117.6kJ/mol;
(g)+H2(g),△H=+117.6kJ/mol; +CO(g)+H2O(g) △H=+158.8 kJ/mol
+CO(g)+H2O(g) △H=+158.8 kJ/mol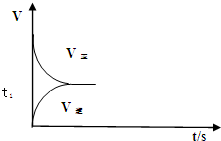
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①②④⑤ | C. | ①②④⑤⑥ | D. | ①③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有Na2O | B. | 只有Na2O2 | C. | Na2O和Na2O2 | D. | 无法确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com