
【题目】将1mol过氧化钠与2mol碳酸氢钠固体混合,在密闭容器中,120℃充分反应后,排出气体,冷却,有固体残留.下列分析正确的是( )
A.残留固体是2mol Na2CO3
B.残留固体是 Na2CO3和NaOH的混合物
C.反应中转移2mol电子
D.排出的气体是1.5mol氧气
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】下列方程式正确的是( )
A.用铁丝网作电极,电解饱和食盐水:2Cl﹣+2H2O![]() 2OH﹣+Cl2↑+H2↑
2OH﹣+Cl2↑+H2↑
B.Ba(OH)2溶液中加入过量的Al2(SO4)3溶液:3Ba2++6OH-+2Al3++3SO42-→3BaSO4↓+2Al(OH)3↓
C.向H218O中投入Na2O2固体: 2H218O + 2Na2O2→ 4Na+ + 4OH-+ 18O2↑
D.石灰乳中Ca(OH)2的电离:Ca(OH)2(s) ![]() Ca2++ 2OH-
Ca2++ 2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过渡元素铁可形成多种配合物,如黄血盐[K4Fe(CN)6]、普鲁士蓝、血红素等
(1)已知:3K4Fe(CN)6]=2KCN + Fe3C + 3C + (CN)2↑ +2N2↑
①(CN)2分子中σ键和π键的数目比为n(σ)﹕n(π)=____。
②(CN)2在一定条件下氢化可以得到乙二胺(H2NCH2CH2NH2),乙二胺易溶于水,除因为是极性分子外,还可能的原因是____。
(2)普鲁士蓝的化学式为Fe4[Fe(CN)6]3,写出外界离子基态核外电子排布式____。
(3)血红素(如图)是血红蛋白的合成原料之一,血红色中的N原子的杂化类型为____,请用“→”在图中标出Fe2+的配位键_________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某柔性屏手机的柔性电池以碳纳米管做电极材料,以吸收ZnSO4溶液的有机高聚物做固态电解质,其电池总反应为:
MnO2+![]() Zn+(1+
Zn+(1+![]() )H2O+
)H2O+![]() ZnSO4
ZnSO4![]() MnOOH+
MnOOH+![]() ZnSO4[Zn(OH)2]3·xH2O
ZnSO4[Zn(OH)2]3·xH2O
其电池结构如图1所示,图2是有机高聚物的结构片段。

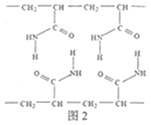
下列说法中,正确的是( )
A.碳纳米管具有导电性,可用作电极材料
B.放电时,电池的正极反应为MnO2-e-+H+=MnOOH
C.充电时,Zn2+移向MnO2
D.合成有机高聚物的单体是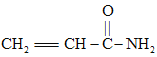
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用浓盐酸与浓硫酸混合快速制取HCl.下列解释合理的是( )
A.浓硫酸是高沸点的酸,通过它与浓盐酸反应制取低沸点的酸
B.通过改变温度和浓度等条件,利用平衡移动原理制取HCl
C.两种强酸混合,溶解度会相互影响,低溶解度的物质析出
D.浓硫酸的浓度远大于浓盐酸的浓度,高浓度的酸制取低浓度的酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卡巴拉丁F是老年人认知障碍的重要治疗药物。其合成路线如图所示:
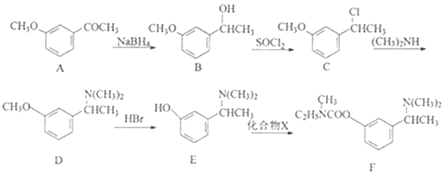
(1)B中含氧官能团的名称为___。
(2)B→C的反应类型为___。
(3)化合物X(C4H3ONCl)的结构简式为__。
(4)写出同时满足下列条件的A的一种同分异构体的结构简式:__。
①能水解,水解产物之一能与FeCl3溶液发生显色反应。
②分子中含有4种不同化学环境的氢。
(5)已知:RX![]() RCN
RCN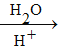 RCOOH
RCOOH
RX+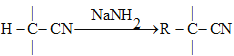
以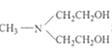 和苯为主要原料制备
和苯为主要原料制备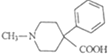 ,写出相应的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。___
,写出相应的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种短周期主族元素,它们的原子序数依次增大,其中B是地壳中含量最多的元素。已知A、C及B、D分别是同主族元素,且B、D两元素原子核内质子数之和是A、C两元素原子核内质子数之和的2倍;在处于同周期的C、D、E三种元素中,E的原子半径最小;通常情况下,五种元素的单质中有三种气体,两种固体。
(1)A为______(填元素符号,下同),B为______,C为______;D的原子结构示意图为______。
(2)试比较D、E两元素的最高价氧化物对应水化物的酸性强弱:______![]() ______(填化学式)。
______(填化学式)。
(3)A和B可形成原子个数比为![]() 的化合物,其化学式为______。
的化合物,其化学式为______。
(4)将E的单质通入A、B、C三种元素组成的化合物的水溶液中,试写出该反应的化学方程式:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锡有SnCl2、SnCl4两种氯化物.SnCl4是无色液体,极易水解,熔点﹣36℃,沸点114℃,金属锡的熔点为231℃.实验室用熔融的金属锡跟干燥的氯气直接作用制取无水SnCl4(此反应过程放出大量的热).实验室制取无水SnCl4的装置如图所示.
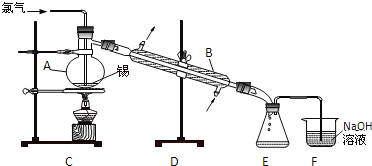
完成下列填空:
(1)仪器A的名称__; 仪器B的名称__.
(2)实验室制得的氯气中含HCl和水蒸气,须净化后再通入液态锡中反应,除去HCl的原因可能是__;除去水的原因是__.
(3)当锡熔化后,通入氯气开始反应,即可停止加热,其原因是__.若反应中用去锡粉11.9g,反应后在锥形瓶中收集到23.8g SnCl4,则SnCl4的产率为__.
(4)SnCl4遇水强烈水解的产物之一是白色的固态二氧化锡.若将SnCl4少许暴露于潮湿空气中,预期可看到的现象是__.
(5)已知还原性Sn2+>I﹣,SnCl2也易水解生成难溶的Sn(OH)Cl.如何检验制得的SnCl4样品中是否混有少量的SnCl2?__.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2违法排放会造成酸雨,可用以下方法处理尾气中的SO2。
方法一:活性炭还原法
2C(s) +2SO2(g) S2(g)+2CO2(g) +Q(Q>0)
一定条件下,各物质浓度与时间的关系如图:
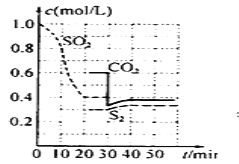
(1)写出该反应的平衡常数表达式:___,第一次达到平衡的时间是第___min。
(2)0-20min化学反应速率表示v(SO2)=___。
(3)若60min时温度升高,CO2气体的浓度将___(填“变大”、“变小”或“不变”)。
(4)30min时平衡发生移动的条件是___。
方法二:亚硫酸钠吸收法
(5)Na2SO3溶液吸收SO2的离子方程式为:___。
(6)常温下,当Na2SO3完全转化为NaHSO3时,溶液中相关离子浓度关系为:(填“>”、”=”或”<”)
c(Na+)+c(H+)___c(SO32-)+c(HSO3-)+c(OH-)
c(Na+)___c(SO32-)+c(HSO3-)+c(H2SO3)
(7)NaHSO3溶液中存在SO32-的原因:___;NaHSO3溶液中存在H2SO3的原因:___;NaHSO3溶液呈酸性,请根据以上分析解释原因:___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com