
【题目】现有部分短周期元素的性质或原子结构如下表:
元素符号 | 元素性质或原子结构 |
T | M层上的电子数是原子核外电子层数的2倍 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
Z | 元素最高正价是+7价 |
下列叙述中不正确的是( )
A.14X可用与测定文物年代
B.Z的非金属性比T强
C.Y和T位于同一主族
D.X元素形成的化合物种类很多
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:
【题目】下图分别表示生物体内生物大分子的部分结构模式图,据图回答:
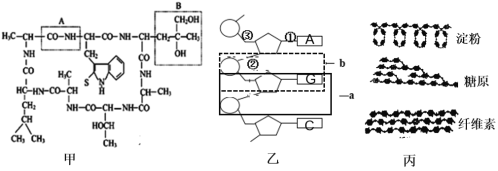
(1)从甲、乙、丙可以看出,生物大分子都是以_________为基本骨架。甲图中A结构名称为__________。
(2)乙图所示化合物的基本组成单位是_____________,各单体间通过_______(用序号表示)相连。如果该链表示RNA的一部分结构,则图示未表示出来的含氮碱基名称是___________ ;如果该链表示DNA的一部分结构,则图示未表示出来的含氮碱基名称是___________ ,图b表示的核苷酸名称为__________________________。
(3)丙图所示三种物质中,在功能上与另外两种截然不同的物质是_________,它可以参与植物细胞中__________(填某细胞结构)的构成 。丙图中三种物质的单体都是__________,该物质为还原糖,常用__________检测;而甲一般用____________检测,两种试剂使用方法的区别是前者需要__________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z在周期表中的位置关系如图所示,已知X最外层电子数为2,则下列叙述中正确的是( )
X | ||
Y | ||
Z |
A.Z一定是活泼的金属元素
B.Y的氢化物稳定性大于Z的氢化物稳定性
C.1molX的单质跟足量水反应时,发生转移的电子为2mol
D.Y的最高价氧化物的水化物是一种强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1mol某有机物M含碳原子 n mol,在恰好完全燃烧时消耗氧气1.5n mol。请把符合条件的物质类别填入空格。
供选择的物质类别有:烷烃、烯烃、炔烃、二烯烃、环烷烃、芳香烃、饱和一元醇、饱和一元醛、醚、酮。
(1)有机物M可能是(填物质的类别)_____________、_____________、_____________、_____________(你认为有几种填几种,但多填少填要扣分)。
(2)若 4.4克M与足量的金属钠反应可收集到560 ml氢气(标准状况),则有机物M一定是(填物质的类别)____________,且M的摩尔质量为___________________。
(3)具有支链的化合物A的分子式为C4H6O2,A可以使溴的四氯化碳溶液褪色。1molA和1mol NaHCO3能完全反应,则A的结构简式是________________________。
(4)化合物B含有C、H、O三种元素,相对分子质量为60,其中碳的质量分数为60%,氢的质量分数为13.33%。B在Cu的催化作用下被氧气氧化成C,C能发生银镜反应,则C发生银镜反应的化学方程式为__________________________。
(5)D在NaOH水溶液中加热反应,可生成A的钠盐和B,相应反应的化学方程式是_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤及硫酸工业尾气中的SO2是重要的大气污染物,可以用以下方法处理尾气中的SO2,
方法一:通过活性炭作用回收
2C(s)+2SO2(g)![]() S2(g)+2CO2(g)
S2(g)+2CO2(g)
(1)上述反应的化学平衡常数表达式为 _____________________;若在某密闭容器中进行上述反应,为了加快吸收SO2,可采取的措施有_____________________________________。
方法二:利用亚硫酸钠溶液进行吸牧
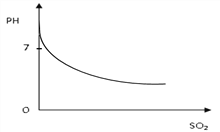
(2)把尾气(含二氧化硫)不断通入到饱和亚硫酸钠溶液中,生成亚硫酸氢钠,pH值的变化如图所示,请根据图示,解释PH值变化的原因:_______________________________________。
方法三:利用氯气和干燥的二氧化硫在活性炭催化剂存在下反应制取氯化硫酰:氯化硫酰(SO2Cl2)主要用作氯化剂。它是一种无色液体,熔点–54.1℃,沸点69.1℃。
SO2(g)+Cl2(g)![]() SO2Cl2(l)+97.3kJ
SO2Cl2(l)+97.3kJ
(3)若反应的容器体积为2L,2分钟内液体质量增加了2.7克,用二氧化硫表示这两分钟内的化学反应速率______________________。
(4)若在此条件下,提高SO2的转化率,可采取的措施有____________________________________;当_________________________________________时说明上述反应已达到平衡状态。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列有关叙述不正确的是 ( )
A. 标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为7/22.4NA
B. 1 mol甲基(—CH3)所含的电子总数为9NA
C. 0.5mol 1,3-丁二烯分子中含有C=C双键数为 NA
D. 1 mol Cl- 所含的电子数为18NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有四种不同堆积方式的金属晶体的晶胞如图所示,下列有关说法正确的是( )

A. ①为简单立方堆积,②为镁型,③为钾型,④为铜型
B. 每个晶胞含有的原子数分别为:①1个,②2个,③2个,④4个
C. 晶胞中原子的配位数分别为:①6,②8,③8,④12
D. 空间利用率的大小关系为:①<②<③<④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com