
下列依据热化学方程式得出的结论正确的是( )
A.若2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ·mol-1,则H2的燃烧热为241.8 kJ·mol-1
B.若C(石墨,s)===C(金刚石,s) ΔH>0,则石墨比金刚石稳定
C.已知NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) ΔH=-57.4 kJ·mol-1,则20.0 g NaOH固体与稀盐酸完全中和,放出28.7 kJ的热量
D.已知2C(s)+2O2(g)===2CO2(g) ΔH1;2C(s)+O2(g)===2CO(g) ΔH2,则ΔH1>ΔH2
科目:高中化学 来源: 题型:
研究氨氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) K1 ΔH1<0(Ⅰ)
NaNO3(s)+ClNO(g) K1 ΔH1<0(Ⅰ)
2NO(g)+Cl2(g) 2ClNO(g) K2 ΔH2<0(Ⅱ)
2ClNO(g) K2 ΔH2<0(Ⅱ)
(1)4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=________(用K1、K2表示)。
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=________(用K1、K2表示)。
(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2,10 min时反应(Ⅱ)达到平衡。测得10 min内v(ClNO)=7.5×10-3 mol·L-1·min-1,则平衡后n(Cl2)=________mol,NO的转化率α1=________。其他条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率α2________α1(填“>”“<”或“=”),平衡常数K2______(填“增大”“减小”或“不变”)。若要使K2减小,可采取的措施是________。
(3)实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH===NaNO3+NaNO2+H2O。含0.2 mol NaOH的水溶液与0.2 mol NO2恰好完全反应得1 L溶液A,溶液B为0.1 mol·L-1的CH3COONa溶液,则两溶液中c(NO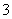 )、c(NO
)、c(NO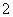 )和c(CH3COO-)由大到小的顺序为____________________________________________。(已知HNO2电离常数Ka=7.1×10-4 mol·L-1,CH3COOH的电离常数Ka=1.7×10-5 mol·L-1)
)和c(CH3COO-)由大到小的顺序为____________________________________________。(已知HNO2电离常数Ka=7.1×10-4 mol·L-1,CH3COOH的电离常数Ka=1.7×10-5 mol·L-1)
可使溶液A和溶液B的pH相等的方法是________。
a.向溶液A中加适量水
b.向溶液A中加适量NaOH
c.向溶液B中加适量水
d.向溶液B中加适量NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MHNi电池)。下列有关说法不正确的是( )
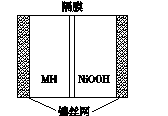
A.放电时正极反应为NiOOH+H2O+e-―→Ni(OH)2+OH-
B.电池的电解液可为KOH溶液
C.充电时负极反应为MH+OH-―→H2O+M+e-
D.MH是一类储氢材料,其氢密度越大,电池的能量密度越高
查看答案和解析>>
科目:高中化学 来源: 题型:
下图所示的电解池Ⅰ和Ⅱ中,a、b、c和d均为Pt电极。电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d。符合上述实验结果的盐溶液是( )
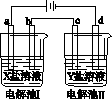
| 选项 | X | Y |
| A. | MgSO4 | CuSO4 |
| B. | AgNO3 | Pb(NO3)2 |
| C. | FeSO4 | Al2 (SO4)3 |
| D. | CuSO4 | AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下简化流程既脱除燃煤尾气中的SO2,又制得电池材料MnO2(反应条件已省略)。
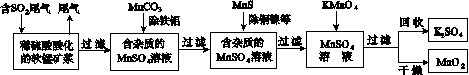
请回答下列问题:
(1)上述流程脱硫实现了____(选填下列字母编号)。
A.废弃物的综合利用
B.白色污染的减少
C.酸雨的减少
(2)用MnCO3能除去溶液中的Al3+和Fe3+,其原因是________________________________。
(3)已知:25 ℃、101 kPa时,
Mn(s)+O2(g)===MnO2(s) ΔH=-520 kJ/mol
S(s)+O2(g)===SO2(g) ΔH=-297 kJ/mol
Mn(s)+S(s)+2O2(g)===MnSO4(s)
ΔH=-1065 kJ/mol
SO2与MnO2反应生成无水MnSO4的热化方程式是____________________________________。
(4)MnO2可作超级电容器材料。用惰性电极电解MnSO4溶液可制得MnO2,其阳极的电极反应式是________________________________。
(5)MnO2是碱性锌锰电池的正极材料。碱性锌锰电池放电时,正极的电极反应式是________________。
(6)假设脱除的SO2只与软锰矿浆中的MnO2反应。按照图示流程,将a m3(标准状况)含SO2的体积分数为b%的尾气通入矿浆,若SO2的脱除率为89.6%,最终得到MnO2的质量为c kg,则除去铁、铝、铜、镍等杂质时,所引入的锰元素相当于MnO2________kg。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
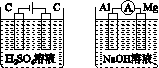
(a) (b)
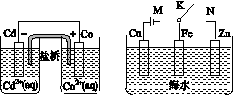
(c) (d)
图G75
A.图(a)中,随着电解的进行,溶液中H+的浓度越来越小
B.图(b)中,Mg电极作电池的负极
C.图(c)中,发生的反应为Co+Cd2+===Cd+Co2+
D.图(d)中,K分别与M、N连接时,Fe电极均受到保护
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式书写正确的是
A.钠和水反应: Na+H2O=Na++OH-+H2↑
B.盐酸与氢氧化钠溶液反应: H++OH-=H2O
C.三氯化铁腐蚀印刷线路板: Fe3++Cu=Fe2++Cu2+
D.盐酸与碳酸钙反应制备二氧化碳: CO32-+2H+=CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生活
(1)(5分)食品和药品关系到人的生存和健康
现有下列五种物质:
A.亚硝酸钠 B.碳酸氢钠 C.苹果汁 D.胡萝卜素 E.阿司匹林
请按下列要求填空(填序号)
常可用于食品防腐的是 ▲ ;富含维生素C的是 ▲ ;用作食品色素的是
▲ ;既可以用于面包的膨松剂,又可以用于治疗胃酸过多的是 ▲ ;可以解热
镇痛的药物是 ▲ 。
(2)(5分)人类的生活离不开材料
①生产硅酸盐水泥和普通玻璃都需要用到的一种主要原料是 ▲ 。
②塑料广泛应用与生产、生活的各个领域,聚乙烯塑料属于 ▲ (填序号)
A.有机高分子材料 B.无机非金属材料 C.金属材料
③蚕丝、尼龙、棉花这三种常见的纤维中,主要成分为蛋白质的是 ▲ 。
④钢铁是使用量最大的金属材料,写出工业炼铁的主要化学反应方程式:
▲ 。
(3)(5分)我们赖以生存的地球只有一个,爱护环境人人有责
①有报道称,国家将投入50亿治理津京地区的“雾霾”。下列措施不能改善“雾霾”
的是 ▲ (填序号)
A.改善机动车燃油的品质 B.严格控制工厂废气的排放
C.学校遇雾霾天气停课放假 D.平时出行,多乘坐公共交通工具
②为了减少燃煤SO2的排放造成的酸雨,常采取一系列的措施,下列措施不能达到目
的的是 ▲ 。
A.燃烧高品质的煤炭 B.用天然气代替燃煤
C.在燃煤中添加石灰石 D.加高燃煤企业的烟囱
③我国淡水资源不但短缺,而且还被大量污染,下列有关水资源的保护正确的是 ▲
A.富含氮、磷的生活污水,不需处理可以直接排放
B.电镀产生的含有重金属离子的废水,可采用高压水泵直接压入地下深层
C.轧钢厂排出含盐酸的废水,可用氢氧化钡中和处理
D.天然水中的小悬浮颗粒,可用明矾等混凝剂净化
④某工厂排放的污水中含有大量的铬元素,某兴趣小组探究含铬(Cr2O72-)废水的处
理方法,经查阅资料,拟采用(NH4)2Fe(SO4)2将Cr2O72-还原为Cr3+,再用氨水将
Cr3+转变为Cr(OH)3,该方案运用了污水处理方法中的氧化还原法和 ▲ ;
指导老师指出该方案处理后的废水中含有大量的 ▲ (填离子符号),能导致 水体富营养化。
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的一部分,下列有关说法正确的是( )
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | cd | ||||||
| 3 | abef |
A.a、b两元素的单质构成原电池两极时,a一定为负极
B.e的氢化物分子和d的氢化物分子不可能含有相同的电子数
C.六种元素中,c元素与其他三种非金属元素均能形成化合物
D.c、e、f的含氧酸的酸性依次增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com