
| A. | 可用高锰酸钾溶液鉴别甲苯、环己烯与溴苯 | |
| B. | 淀粉与纤维素互为同分异构体,二者水解的最终产物相同 | |
| C. | 石油裂解和油脂皂化都是由高分子化合物生成小分子物质的过程 | |
| D. | 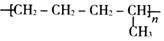 是由单体CH2=CH-CH3和CH2=CH2发生加聚反应的产物 是由单体CH2=CH-CH3和CH2=CH2发生加聚反应的产物 |
分析 A.甲苯、环己烯与高锰酸钾都反应;
B.淀粉与纤维素不是同分异构体;
C.油脂不是高分子化合物;
D.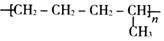 可由CH2=CH-CH3和CH2=CH2发生加聚反应生成.
可由CH2=CH-CH3和CH2=CH2发生加聚反应生成.
解答 解:A.甲苯、环己烯与高锰酸钾都反应,可用溴水鉴别,故A错误;
B.淀粉与纤维素都为高分子化合物,聚合度介于较大范围之间,二者分子式不一定相同,不是同分异构体,故B错误;
C.油脂的相对分子质量较小,不是高分子化合物,故C错误;
D.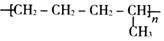 可由CH2=CH-CH3和CH2=CH2发生加聚反应生成,故D正确.
可由CH2=CH-CH3和CH2=CH2发生加聚反应生成,故D正确.
故选D.
点评 本题考查有机物的结构和性质,为高频考点,侧重考查学生的分析能力,注意把握有机物的组成、结构和官能团的性质,本题注意高聚物单体的判断,把握高分子化合物的特点,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
| 实验序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| CO2体积(mL) | 2352 | 2352 | 2352 | 2352 |
| 样品体积(mL) | 20.0 | 30.0 | 40.0 | 50.0 |
| 沉淀物质的量(×10-2mol) | 1.50 | 4.50 | 6.00 | 7.50 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2LCCl4中含有的分子数目为0.5NA | |
| B. | 25℃,1.01×105Pa,16gO2和O3的混合气体中含有的原子数NA | |
| C. | 常温下,5.6g铁完全溶解于稀盐酸,铁失去的电子数为0.3 NA | |
| D. | 标准状况下,22.4LN2和CO混合气中含4NA个原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用分液漏斗分离除去溴苯中混入的溴 | |
| B. | 顺-2-丁烯和反-2-丁烯的加氢产物不同 | |
| C. | 石油的裂解是化学变化,而石油的分馏和煤的干馏是物理变化 | |
| D. | 结构简式为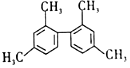 的分子中至少有11个碳原子处于同一平面上 的分子中至少有11个碳原子处于同一平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 编号 | 电极材料 | 电解制溶液 | 电流指针偏转方向 |
| 1 | Mg Al | 稀盐酸 | 偏向Al |
| 2 | Al Cu | 稀盐酸 | 偏向Cu |
| 3 | Al 石墨 | 稀盐酸 | 偏向石墨 |
| 4 | Mg Al | NaOH溶液 | 偏向Mg |
| 5 | Al Zn | 浓硝酸 | 偏向Al |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
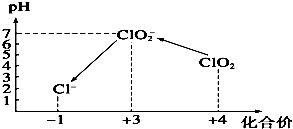 ClO2气体是一种常用的消毒剂,我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒.
ClO2气体是一种常用的消毒剂,我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 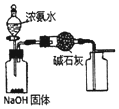 用图装置,制取干燥纯净的NH3 | |
| B. |  用图装置,实验室制备Fe(OH)2 | |
| C. | 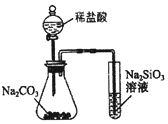 用图所示实验,可比较氯、碳、硅三种元素的非金属性强弱 | |
| D. | 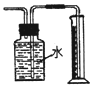 用图装置测量Cu与浓硝酸反应产生气体的体积 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com