
【题目】在一定温度下,将2 mol SO2和1 mol O2充入一定容积的密闭容器中,在催化剂作用下发生反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-197kJ/mol,下列说法中正确的是
2SO3(g) ΔH=-197kJ/mol,下列说法中正确的是
A.为提高SO2转化率,可以再加入SO2B.平衡时放出197kJ热量
C.平衡时再充入O2,则v正增大,v逆减小D.平衡时SO2和SO3共2mol
 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:
【题目】锶有“金属味精”之称。以天青石(主要含有SrSO4和少量CaCO3、MgO杂质)生产氢氧化锶的工艺如下:

已知氢氧化锶在水中的溶解度:
温度(℃) | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
溶解度(g/100mL) | 0.91 | 1.25 | 1.77 | 2.64 | 3.95 | 8.42 | 20.2 | 44.5 | 91.2 |
(1)隔绝空气焙烧时SrSO4只被还原成SrS,化学方程式为____。
(2)“除杂”方法:将溶液升温至95℃,加NaOH溶液调节pH为12。
①95℃时水的离子积KW=1.0×10-12,Ksp[Mg(OH)2]=1.2×10-10,则溶液中c(Mg2+)=____。
②若pH过大,将导致氢氧化锶的产率降低,请解释原因____。
(3)“趁热过滤”的目的是____,“滤渣”的主要成分为___。
(4)从趁热过滤后的滤液中得到Sr(OH)2产品的步骤为____、过滤、洗涤、干燥。
(5)“脱硫”方法:用FeCl3溶液吸收酸浸产生的气体,吸收时的氧化产物为___(填化学式);再用石墨电极电解吸收液,电解后可在“脱硫”中循环利用的物质是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于A(g)+2B(g)![]() 3C(g)的化学反应,下列表示的反应速率最快的是( )
3C(g)的化学反应,下列表示的反应速率最快的是( )
A. v(A)=0.6 mol/(L·min) B. v(B)=0.3 mol/(L·s)
C. v(C)=0.9 mol/(L·min) D. v(C)=1.2 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于镁、铝的说法正确的是( )
A. 铝制品在空气中能稳定存在是因为铝不活泼
B. 浓HNO3、浓H2SO4能用铝制器皿盛装是因为铝与浓HNO3、浓H2SO4不反应
C. 镁、铝均能与NaOH溶液反应
D. 铝与Fe2O3发生铝热反应是利用了Al的还原性比Fe强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表达下列反应的离子方程式为
A. 用醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O
B. 硫化亚铁与浓硫酸混合加热:2H++FeS=H2S↑+ Fe2+
C. 向硫酸铝溶液中滴加碳酸钠溶液:2Al3++3![]() =Al2(CO3)3↓
=Al2(CO3)3↓
D. 用氢氧化钠溶液吸收工业废气中的NO2:2NO2+2OH-=![]() +
+![]() + H2O
+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NO2和N2O4之间发生反应:N2O4![]() 2NO2,一定温度下,体积为2L的密闭容器中,各物质的物质的量随时间变化的关系如图所示。请回答下列问题:
2NO2,一定温度下,体积为2L的密闭容器中,各物质的物质的量随时间变化的关系如图所示。请回答下列问题:
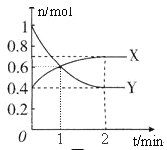
(1)曲线____________(填“X”或“Y”)表示NO2的物质的量随时间的变化曲线。在0到1min中内用X表示该反应的速率是________________,该反应达最大限度时Y的转化率_______。
(2)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中 v(NO2)=0.3 mol·L-1·min-1,乙中y(N2O4)=0.2 mol·L-1·min-1,则__________中反应更快。
(3)下列描述能表示反应达平衡状态的是______________________。
A.容器中X与Y的物质的量相等
B.容器内气体的颜色不再改变
C.2v(X)=v(Y)
D.容器内气体的平均相对分子质量不再改变
E.容器内气体的密度不再发生变化
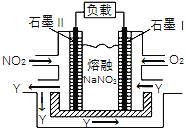
(4)NO2、O2和熔融NaNO3可制作燃料电池,其原理如右图,该电池在使用过程中石墨Ⅱ电极上生成氧化物Y(N2O5),则石墨I电极是______________(填“正极”或“负极”),石墨Ⅱ的电极反应式为_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库:从海水中提取食盐和溴的过程如下:
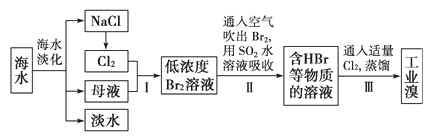
下列说法错误的是
A.海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等
B.电解熔融的氯化钠是一个将电能转化为化学能的过程
C.步骤Ⅱ中将Br2还原为Br-的目的是富集溴元素
D.向母液中加入石灰乳可得到Mg(OH)2,工业上常用电解熔融的Mg(OH)2来制取镁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示一定温度下,在容积固定的密闭容器中,A、B、C三种气体的物质的量浓度随时间变化的情况。回答下列问题:

(1)该反应的化学方程式为_________。
(2)0~t1s内,B气体的平均反应速率为____。
(3)(t1+10)s时,A气体的转化率为__________,此时v正(A)_____v逆(B)(填“>”“<”或“=")。
(4)下列关于该反应的说法正确的是__________(填标号)。
a.t1时刻,该反应的正反应和逆反应均已停止
b.t1时刻之前,B气体的消耗速率大于它的生成速率
c.t1时刻,C气体的正反应速率等于它的逆反应速率
(5)容器中,(t1+10)s时的压强与起始时的压强之比为____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物Z是一种医药中间体,由X制备Z的物质转化路线如图,下列说法正确的是( )
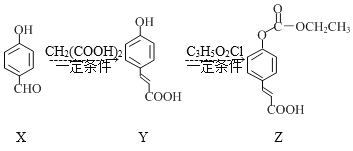
A.X在空气中不易氧化变质
B.可用FeCl3溶液鉴别X、Y
C.1molX最多能与4molH2反应
D.C3H5O2Cl的结构简式为ClCOOC2H5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com