
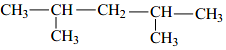 ,该烯烃可能的结构有( )
,该烯烃可能的结构有( )| A. | 1 种 | B. | 2 种 | C. | 3 种 | D. | 4 种 |
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:解答题
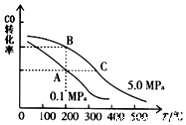 研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义.
研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
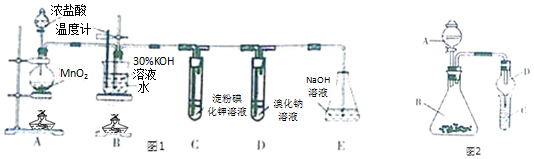
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 向CaC2O4饱和溶液中加入固体Na2C2O4可以由a点变到b点 | |
| B. | 通过蒸发可以由d点变到c点 | |
| C. | d点无CaC2O4沉淀生成 | |
| D. | a点对应的Ksp大于c点对应的Ksp |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
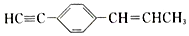 的说法中不正确的是( )
的说法中不正确的是( )| A. | 最多只有5个碳原子在同一直线上 | B. | 最多有11个碳原子在同一平面上 | ||
| C. | 有7个碳原子可能在同一直线上 | D. | 最多有19个原子在同一平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 废旧印刷电路板的回收利用可实现资源再生,并减少污染.废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末.
废旧印刷电路板的回收利用可实现资源再生,并减少污染.废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com