
 甲醇与水蒸气反应:CH3OH(g)+H2O$\stackrel{催化剂}{?}$CO2(g)+3H2(g).
甲醇与水蒸气反应:CH3OH(g)+H2O$\stackrel{催化剂}{?}$CO2(g)+3H2(g).| 0min | 10min | 20min | 60min | 70min | |
| c(H2O)/mol•L-1 | 3.00 | 2.80 | 2.65 | 2.50 | 2.50 |
| c(CH3OH)/mol•L-1 | 1.00 | 0.80 | 0.65 | 0.50 | 0.50 |
| 实验编号 | T/℃ | c(CH3OH)/mol•L-1 | c(H2O)/mol•L-1 | 催化剂 |
| Ⅰ | 280 | 1.00 | 3.00 | CuO |
| Ⅱ | X | 1.00 | 3.00 | ZrO2 |
| Ⅲ | 380 | Y | Z | ZrO2 |
分析 (1)①根据v=$\frac{△c}{△t}$计算v(H2O);
②60min处于平衡状态,计算甲醇浓度变化量,甲醇转化率=$\frac{甲醇浓度变化量}{甲醇起始浓度}$×100%;
③计算平衡时各组分浓度,代入平衡常数表达式K=$\frac{c(C{O}_{2})×{c}^{3}({H}_{2})}{c(C{H}_{3}OH)×c({H}_{2}O)}$计算;
(2)①实验目的是:探究不同催化剂、温度对化学反应速率的影响,采取控制变量法,实验Ⅰ与实验Ⅱ催化剂不同,实验Ⅱ、Ⅲ温度不同,其它条件相同;
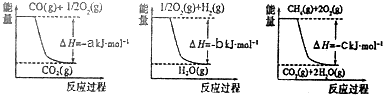
②由图可知,温度越高平衡时甲醇的浓度越小,说明升高温度平衡正向移动;
③控制条件应符合反应速率快且甲醇的转化率大.
解答 解:(1)①0-10min内水的浓度变化量为(3-2.8)mol/L=0.2mol/L,则v(H2O)=$\frac{0.2mol/L}{10min}$=0.02 mol•L-1•min-1,故答案为:0.02 mol•L-1•min-1;
②60min处于平衡状态,平衡时甲醇浓度变化量为(1-0.5)mol/L=0.5mol/L,则甲醇转化率=$\frac{0.5mol/L}{1mol/L}$×100%=50%,故答案为:50%;
③60min处于平衡状态,平衡时甲醇浓度变化量为0.5mol/L,则:
CH3OH(g)+H2O?CO2(g)+3H2(g)
起始量(mol/L):1 3 0 0
变化量(mol/L):0.5 0.5 0.5 1.5
平衡量(mol/L):0.5 2.5 0.5 1.5
平衡常数K=$\frac{c(C{O}_{2})×{c}^{3}({H}_{2})}{c(C{H}_{3}OH)×c({H}_{2}O)}$=$\frac{0.5×1.{5}^{3}}{0.5×2.5}$=1.35,
故答案为:1.35;
(2)①实验目的是:探究不同催化剂、温度对化学反应速率的影响,采取控制变量法,实验Ⅰ与实验Ⅱ催化剂不同,实验Ⅱ、Ⅲ温度不同,则X为280,Y为1.00,Z为3.00,
故答案为:280;1.00;3.00;
②由图可知,温度越高平衡时甲醇的浓度越小,说明升高温度平衡正向移动,正反应为吸热反应,故△H>0,故答案为:>;
③由图可知温度高,甲醇的转化率大,而ZrO2的催化效果比CuO好,故选择条件为:380℃,ZrO2做催化剂,
故答案为:380℃,ZrO2做催化剂.
点评 本题考查化学平衡计算、平衡常数、化学平衡影响因素、影响反应速率因素探究等,(2)注意利用控制变量法分析解答,难度中等.


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:选择题
| A. | AlCl3溶液蒸干、灼烧至恒重,最终剩余固体是AlCl3 | |
| B. | 在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大 | |
| C. | 将纯水加热至较高温度,KW变大、pH变小、呈酸性 | |
| D. | 锅炉中沉积的CaSO4可用饱和Na2CO3溶液浸泡,再将不溶物用稀盐酸溶解除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ②③④⑤ | C. | ②③④ | D. | ②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| T/min | 0 | 1 | 2 | 3 | 4 |
| n(H2O)/mol | 1 | 0.8 | 0.65 | 0.6 | 0.6 |
| n(CO)/mol | 0.8 | 0.6 | 0.45 | 0.4 | 0.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 3molH2、2molN2 | 6molH2、4molN2 | 2molNH3 |
| 达到平衡的时间(min) | T | 5 | 8 |
| 平衡时N2的浓度(mol•L-1) | C1 | 3 | |
| N2的体积分数 | ω1 | ω2 | ω3 |
| 混合气体密度(g•L-1) | ρ1 | ρ2 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ①③⑤ | C. | ③④⑤ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2溶于水后能导电,故CO2为电解质 | |
| B. | H216O、D216O、H218O、D218O互为同素异形体 | |
| C. | NaCl溶液和CH3COONH4溶液均显中性,故两溶液中水的电离程度相同 | |
| D. | 溶液与胶体本质区别为分散质微粒直径的大小不同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com