
向25mL0.1mol/LNaOH溶液中逐滴加入0.2mol/L醋酸溶液,曲线如下图所示。下列有关溶液中粒子浓度关系的描述中,正确的是( )

A.在A、B间任一点:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.在B点:a =12.5,且有c(Na+)=c(CH3COO-)
C.在C点:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D.在D点:c(CH3COO-) + c(CH3COOH) = 2c(Na+)
科目:高中化学 来源: 题型:
 23.25℃时,向25mL0.1mol?L-1NaOH溶液中逐滴加入0.1mol?L-1 H2B溶液,曲线如图所示,a>12.5.回答下列问题:
23.25℃时,向25mL0.1mol?L-1NaOH溶液中逐滴加入0.1mol?L-1 H2B溶液,曲线如图所示,a>12.5.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
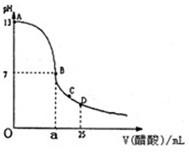 Ⅰ.如图为向25mL0.1mol?L-NaOH溶液中逐滴加入0.2mol?L-醋酸溶液过程中溶液pH的变化曲线,请回答:
Ⅰ.如图为向25mL0.1mol?L-NaOH溶液中逐滴加入0.2mol?L-醋酸溶液过程中溶液pH的变化曲线,请回答:查看答案和解析>>
科目:高中化学 来源:2010-2011学年江苏省苏锡常镇四市高三调研测试(一)化学试卷 题型:选择题
常温下,向25mL0.1mol∙L-1 NaOH溶液中逐滴加入0.1mol∙L-1 CH3COOH溶液,曲线如图所示,有关粒子浓度关系正确的是

A.只有在A、B间任一点,溶液中才有:
c(Na+)+c(H+)=c(CH3COO-)+(OH-)
B.在B点,a>25,且有c(Na+)=c(CH3COO-)>c(OH-)=c(H+)
C.在C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
D.在D点:c(CH3COO-)+c(CH3COOH)=c(Na+)
查看答案和解析>>
科目:高中化学 来源:2013届黑龙江省高二上学期期末考试化学试卷 题型:选择题
室温下,向25mL0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,混合溶液的pH随加入醋酸体积的变化曲线如图所示,若忽略两溶液混合时的体积变化,下列有关粒子浓度关系错误的是

A.在A、B间任意一点,溶液中一定都有c(Na+) + c(H+) = c(CH3COO-) + c(OH-)
B.在B点:a>12.5,且有c(Na+) = c(CH3COO-)>c(H+) = c(OH-)
C.在C点:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D.在D点:c(CH3COO-) + c(CH3COOH) = 0.1 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com