
设NA为阿伏加德罗常数值,下列有关叙述正确的是( )
A. 标准状况下,2.24 LSO3含有的分子数为0.1NA。
B. 标准状况下,5.6LCO2与足量Na2O2反应转移的电子数为0.5NA。
C. 1 molFe溶于过量硝酸,电子转移数为2NA。
D. 2.0gH218O与D2O的混合物中所含中子数为NA 。
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源:2017届云南省高三下学期第一次统测理综化学试卷(解析版) 题型:选择题
下列说法错误的是
A. Na2O2可用作供氧剂
B. Al2O3可用作耐火材料
C. 地沟油经处理后可用作燃料油
D. 胶体和溶液的本质区别是胶体具有丁达尔现象
查看答案和解析>>
科目:高中化学 来源:2017届江西省九江市十校高三第二次联考理科综合化学试卷(解析版) 题型:填空题
A、B、C、D为原子序数依次增大的四种元索,A2-和B+具有相同的电子构型;C、 D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是 (填元素符号),其中C原子的核外电子排布布式为 。
(2)单质A有两种同素异形体,其中沸点高的是 (填分子式),原因是 ;A和B的氢化物所属的晶体类型分别为 和 。
(3)C和D反应可生成组成比为1:3的化合物E, E的立体构型为 ,中心原子的杂化轨道类型为 。
(4)化合物D2A的立体构型为 ,中心原子的价层电子对数为 ,单质D与湿润的Na2CO3反应可制备D2A,其化学方程式为 。
(5)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数,a=0.566nm,F 的化学式为 :晶胞中A 原子的配位数为 ;列式计算晶体F的密度(g.cm-3) 。
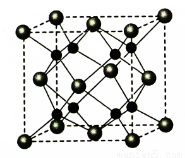
查看答案和解析>>
科目:高中化学 来源:2017届湖南省衡阳市高三实验班第六次月考理综化学试卷(解析版) 题型:选择题
短周期主族元素X、Y、Z、W的原子序数依次增大,原子半径:r(W)>r(Y)>r(Z)>r(X)。X与W同主族,Z原子最外层电子数是其内层电子总数的3倍,Z原子的核电荷数等于X、Y原子核电荷数之和。下列说法正确的是
A. 元素Z、W的简单离子的电子层结构不同
B. 元素Y的简单气态氢化物的热稳定性比Z的强
C. 仅由X、Y、Z三种元素形成的化合物的水溶液可能呈碱性
D. 化合物X2Z2与W2Z2所含化学键类型完全相同
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一3月月考化学试卷(解析版) 题型:填空题
按要求填空:
(1)硫酸在下列用途或反应中各表现的性质是(用字母填在横线上)。
A.难挥发性 B.强酸性 C.吸水性 D.脱水性 E.强氧化性
①浓硫酸可用作气体干燥剂_______;
②往晶体硫酸铜中加浓硫酸,晶体变白______;
③浓硫酸与铜反应______;
④运用铁制槽车和铝制槽车运输浓硫酸_______;
⑤蔗糖中加入浓硫酸,形成“黑色发糕”_______;
⑥浓硫酸使润湿蓝色石蕊试纸先变红后又变黑_______;
⑦浓硫酸和浓氨水反应没有白烟现象_______;
(2)写出上题(1)中对应序号的主要化学方程式③浓硫酸与铜反应____________________,⑤蔗糖中加入浓硫酸,形成“黑色发糕”_________________
(3)请写出稀释浓硫酸的正确操作方法_________用过量的锌与浓硫酸反应时,可能产生的气体是____,理由是_______。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省大同市高一3月月考化学试卷(解析版) 题型:填空题
己知H元素有多种同位素。
(1)有H、D (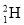 )、T(
)、T(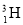 )三种原子,各自可形成双原子分子H2、D2、T2。
)三种原子,各自可形成双原子分子H2、D2、T2。
①标准状况下,它们的密度之比为___________。
②相同物质的量的三种单质中,质子数之比为______________。
③同温同压下,1L各单质气体中所含电子数之比为__________。
(2)36gH2O与80gD2O的物质的量之比是__________,它们分別与Na反应时,所放出气体体积之比(同条件)是__________,质量之比是__________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省大同市高一3月月考化学试卷(解析版) 题型:选择题
几种短周期元素的原子半径及某些化合价见下表。分析判断下列说法正确的是( )
元素代号 | A | B | D | E | G | I | J | K | |
化合价 | -1 | -2 | +4 -4 | +7 -1 | +5 -3 | +3 | +2 | +1 | |
原子半径/ nm | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 | |
A. A的单质是一种常见的还原剂 B. E的含氧酸酸性比D的含氧酸酸性强
C. A、I、J的商子半径由大到小顺序是A>J>I D. A的气态氢化物是强酸
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三3月月考理科综合化学试卷(解析版) 题型:选择题
化学离不开生活,生活也离不开化学。下列叙述中科学的是
A. 广告语“农家肥蔬菜,无公害,绝对不含任何化学物质”
B. 医用酒精是利用了乙醇的氧化性来杀菌消毒的
C. 面食加工时加入少量苏打粉时是防止酸败,加入少量小苏打粉时是作膨松剂
D. 空气质量日报中计入污染指数的项目为可吸入颗粒物、SO2、NOx、CO2
查看答案和解析>>
科目:高中化学 来源:2017届新疆乌鲁木齐地区高三第二次诊断性测验化学试卷(解析版) 题型:简答题
硫酸铅(PbSO4)广泛应用于制造铅蓄电池、白色颜料等。利用方铅矿精矿( PbS)直接制备硫酸铅粉末的流程如下:
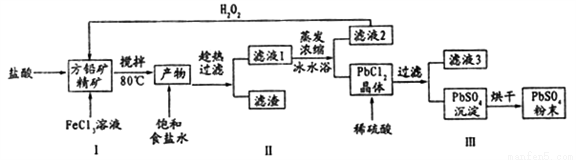
已知:(i) PbCl2 (s)+2C1-(aq)=PbCl42-(aq) △H>0
(ii)有关物质的Ksp和沉淀时的pH如下:
物质 | Ksp | 物质 | 开始沉淀时pH | 完全沉淀时pH |
PbSO4 | 1.0×10-8 | Fe(OH)3 | 2.7 | 3.7 |
PbCl2 | 1.6×10-5 | Pb(OH)2 | 6 | 7.04 |
(1)步骤I反应加入盐酸后可以观察到淡黄色沉淀生成,请写出的离子方程式___________。
(2)用化学平衡移动的原理解释步骤Ⅱ中使用冰水浴的原因____________。
(3)在上述生产过程中可以循环利用的物质有______________。
(4)写出步骤Ⅲ中PbCl2晶体转化为PbSO4沉淀的离子方程式________________。
(5)铅的冶炼、加工会使水体中重金属铅的含量增大造成严重污染。某课题组制备了一种新型脱铅剂(用EH表示),能有效去除水中的痕量铅,脱铅过程中主要发生的反应为:2EH(s)+Pb2+ E2Pb(s)+2H+。则脱铅的最合适的pH范围为____(填编号)
E2Pb(s)+2H+。则脱铅的最合适的pH范围为____(填编号)
A.4~5 B.6~7 C.9~10 D.11~12
(6)PbSO4热激活电池可用作火箭、导弹的工作电源。基本结构如图所示,其中作为电解质的无水LiCl-KC1混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。
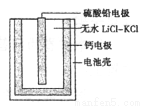
①放电过程中,Li+向_______移动(填“负极”或“正极”)。
②负极反应式为_____________。
③电路中每转移0.2mol电子,理论上生成_________g Pb。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com