


科目:高中化学 来源: 题型:
| A、正极电极反应:O2+2H2O+4e-?4OH- | B、负极电极反应:CH3OH+8OH--6e-?CO32-+6H2O | C、电池在使用过程中电解质溶液的pH升高 | D、当外电路通过0.6 mol电子时,理论上消耗甲醇3.2 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
(2009河北石家庄一模,29)最新研制的一种由甲醇和氧气以及强碱作电解质溶液的新型手机电池。下列有关此电池的叙述错误的是( )
A.正极电极反应:O2+2H2O+4e-====4OH-
B.负极电极反应:CH3OH+8OH--6e-====![]() +6H2O
+6H2O
C.电池在使用过程中电解质溶液的pH升高
D.当外电路通过0.6 mol电子时,理论上消耗甲醇3.2 g
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.正极电极反应:O2+2H2O+4e-=4OH- | ||
B.负极电极反应:CH3OH+8OH--6e-=C
| ||
| C.电池在使用过程中电解质溶液的pH降低 | ||
| D.当外电路通过0.6mol电子时,理论上消耗甲醇6.4g |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省实验中学高三(上)第二次诊断化学试卷(解析版) 题型:选择题
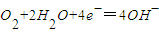
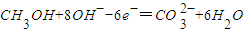
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com