
【题目】已知:乙炔的结构为H—C≡C—H,4个原子在同一直线上,能与单质溴发生加成反应,1,4-二苯基丁二炔广泛应用于农药的合成,其结构如图所示。下列有关该物质的说法不正确的是( )
![]()
A.该有机物的化学式为C16H10
B.该分子中处于同一直线上的原子最多有6个
C.该物质能使溴的四氯化碳溶液褪色
D.该分子中所有原子可能位于同一平面上
科目:高中化学 来源: 题型:
【题目】下刎有关实验装置、操作,不能实现相应实验目的的是

A. 装置甲可用酸性KMnO4溶液滴定FeSO4溶液
B. 用装置乙进行实验时若逐滴滴加AgNO3溶液先出现黄色沉淀,可说明 Ksp(AgCl)>Ksp(AgI)
C. 装置丙可用于收集氢气
D. 装置丁可用于 NaOH溶液除去溴苯中单质溴
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是碳酸钙(CaCO3)在25℃和100℃两种情况下,在水中的沉淀溶解平衡曲线。下列有关说法正确的是

A.CaCO3(s)![]() Ca2+(aq)+CO32—(aq)ΔH<0
Ca2+(aq)+CO32—(aq)ΔH<0
B.a、b、c、d四点对应的溶度积Ksp关系:d﹥b﹥c﹥a
C.25℃时,蒸发溶剂可能使溶液由a点变为曲线上b、c之间的某一点(不含b、c)
D.25℃时CaCO3的Ksp=2.8×10-9,d点无沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36。已知X的一种1∶2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子的s能级与p能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,原子中只有一个未成对电子。
(1)Y原子核外共有________种不同运动状态的电子,基态T原子有________种不同能级的电子。
(2)X、Y、Z的第一电离能由小到大的顺序为_______________(用元素符号表示)。
(3)由X、Y、Z形成的离子ZXY-与XZ2互为等电子体,则ZXY-中X原子的杂化轨道类型为_______________________。
(4)Z与R能形成化合物甲,1 mol甲中含________mol化学键,甲与氢氟酸反应,生成物的分子空间构型分别为___________________。
(5)G、Q、R氟化物的熔点如下表,造成熔点差异的原因为_________________。
氟化物 | G的氟化物 | Q的氟化物 | R的氟化物 |
熔点/K | 993 | 1539 | 183 |
(6)向T的硫酸盐溶液中逐滴加入Y的氢化物的水溶液至过量,反应的离子方程式为___________,
(7)X单质的晶胞如图所示,一个X晶胞中有________个X原子。
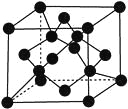
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]端炔烃在催化剂存在下可发生偶联反应,称为Glaser反应。
2R—C≡C—H![]() R—C≡C—C≡C—R+H2
R—C≡C—C≡C—R+H2
该反应在研究新型发光材料、超分子化学等方面具有重要价值。下面是利用Glaser反应制备化合物E的一种合成路线:
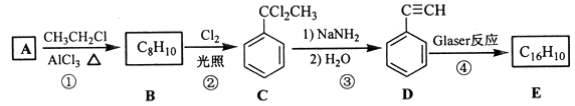
回答下列问题:
(1)B的结构简式为______,D 的化学名称为______。
(2)①和③的反应类型分别为______、______。
(3)E的结构简式为______。用1 mol E合成1,4二苯基丁烷,理论上需要消耗氢气_______mol。
(4)化合物(![]() )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为_____________________________________。
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为_____________________________________。
(5)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3:1,写出其中3种的结构简式_______________________________。
(6)写出用2苯基乙醇为原料(其他无机试剂任选)制备化合物D的合成路线___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(A1N)是一种新型无机非金属材料。某A1N样品仅含有Al2O3杂质,为测定A1N的含量,设计如下三种实验方案。
已知:AlN+NaOH+H2O=NaAlO2+NH3↑
(方案一)
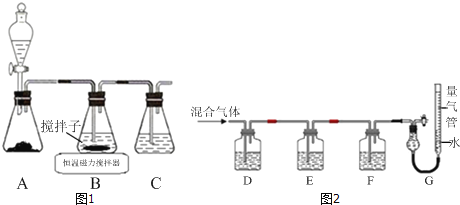
取一定量的样品,用以下装置测定样品中A1N的纯度(夹持装置已略去)。

(1)如图1C装置中球形干燥管的作用是___。
(2)完成以下实验步骤:组装好实验装置,首先___再加入实验药品。接下来的实验操作是___,打开分液漏斗活塞,加入浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化,通入氮气的目的是___。
(3)由于装置存在缺陷,导致测定结果偏高,请提出改进意见____。
(方案二)
用如图2装置测定mg样品中A1N的纯度(部分夹持装置已略去)。
(4)为测定生成气体的体积,量气装置中的X液体可以是___。
a.CCl4 b.H2O c.NH4Cl溶液 d.苯
(5)若mg样品完全反应,测得生成气体的体积为VmL(已转换为标准状况),则A1N的质量分数____。
(方案三)
按如图3步骤测定样品中A1N的纯度:
(6)步骤②生成沉淀的离子方程式为____。
(7)若在步骤③中未洗涤,测定结果将___(填“偏高”“偏低’或“无影响”)。
(8)实验室制取NO2气体。在如图4虚线框内画出用铜与浓硝酸制取和收集NO2的装置简图___(夹持仪器略)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl晶体呈白色,熔点为430℃,沸点为1490℃,见光分解,露置于潮湿空气中易被氧化,难溶于水、稀盐酸、乙醇,易溶于浓盐酸生成H3CuCl4,反应的化学方程式为CuCl(s)+3HCl(aq)H3CuCl4(aq).
(1)实验室用如图1所示装置制取CuCl,反应原理为:
2Cu2++SO2+8Cl﹣+2H2O═2CuCl43﹣+SO![]() +4H+
+4H+
CuCl43﹣(aq)CuCl(s)+3Cl﹣(aq)
①装置C的作用是_____.
②装置B中反应结束后,取出混合物进行如图所示操作,得到CuCl晶体.
混合物![]()
![]()
![]()
![]()
![]() CuCl晶体
CuCl晶体
操作ⅱ的主要目的是_____
操作ⅳ中最好选用的试剂是_____.
③实验室保存新制CuCl晶体的方法是_____.
④欲提纯某混有铜粉的CuCl晶体,请简述实验方案:_____.
(2)某同学利用如图2所示装置,测定高炉煤气中CO、CO2、N2和O2的百分组成.
已知:
i.CuCl的盐酸溶液能吸收CO形成Cu(CO)ClH2O.
ii.保险粉(Na2S2O4)和KOH的混合溶液能吸收氧气.
①D、F洗气瓶中宜盛放的试剂分别是_____、_____.
②写出保险粉和KOH的混合溶液吸收O2的离子方程式:_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业合成氨反应在催化剂表面的反应历程及能量变化如图所示,下列说法正确的是
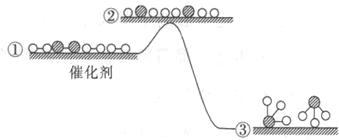
A.增大压强,①→②之间的能量差值会增大
B.合成氨的正逆反应的焓变相同
C.合成氨的过程是吸热反应
D.若使用催化剂,生成等量的NH3需要的时间更短
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标况下,a克气体X与b克气体Y的分子数相同,下列说法错误的是( )
A.X和Y的式量之比是a:b
B.气体X和气体Y的密度比为b:a
C.1g气体X和1g气体Y的分子数之比是a:b
D.1mol气体X和1mol气体Y的质量比是a:b
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com