
 液中,以0.50 mol/L氢氧化钠溶液滴定后得滴定曲线如图所示。
液中,以0.50 mol/L氢氧化钠溶液滴定后得滴定曲线如图所示。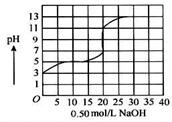
A.该弱酸在滴定前 的浓度是0.15 mol/L 的浓度是0.15 mol/L |
| B.该弱酸稀释10倍后pH为4 |
| C.滴定过程为求滴定终点,最合适的指示剂是酚酞 |
| D.滴定过程为求滴定终点,最合适的指示剂是甲基橙 |
科目:高中化学 来源:不详 题型:单选题
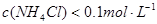 时,溶液的pH
时,溶液的pH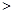 5.1,现用
5.1,现用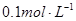 盐酸滴定20mL
盐酸滴定20mL 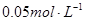 氨水,用甲基橙作指示剂,达到终点时所用盐酸的量是( )
氨水,用甲基橙作指示剂,达到终点时所用盐酸的量是( )| A.10mL | B.5mL | C.大于10mL | D.小于5mL |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1∶10∶100∶1000 | B.0∶1∶12∶11 |
| C.14∶13∶12∶11 | D.14∶13∶2∶3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 温度/℃ | 25 | t1 | t2 |
| Kw/ mol2·L-2 | 1×10-14 | a | 1×10-12 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 1mol·L-1的NaOH溶液的pH为11,则该温度下水的Kw= .(2分)
1mol·L-1的NaOH溶液的pH为11,则该温度下水的Kw= .(2分)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.煤、石油、天然气均为化石能源 |
| B.化石燃料在燃烧过程中能产生污染环境的SO2等有害气体 |
| C.直接燃烧煤不如将煤进行深加工后再燃烧效果好 |
| D.化石能源是可再生能源 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 -1
-1查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com