
| A. | Cu2++2OH-→Cu(OH)2↓ 3CuSO4+2Fe(OH)3→Fe2(SO4)3+3Cu(OH)2↓ | |
| B. | S2-+2Ag+→Ag2S↓ H2S+2AgNO3→Ag2S↓+2HNO3 | |
| C. | CO32-+2H+→H2O+CO2↑ Na2CO3+2CH3COOH→2CH3COONa+H2O+CO2↑ | |
| D. | Ag++Cl-=AgCl↓ AgNO3+NaCl=NaNO3+AgCl↓ |
分析 A.CuSO4与Fe(OH)3不反应;
B.H2S在离子反应中保留化学式,且Ag2S、HNO3可发生氧化还原反应;
C.CH3COOH在离子反应中保留化学式;
D.AgNO3+NaCl=NaNO3+AgCl↓的离子反应为Ag++Cl-=AgCl↓.
解答 解:A.CuSO4与Fe(OH)3不反应,Cu2++2OH-=Cu(OH)2↓表示可溶性铜盐与强碱反应生成氢氧化铜和可溶性盐的反应,故A不选;
B.H2S在离子反应中保留化学式,且Ag2S、HNO3可发生氧化还原反应,则S2-+2Ag+=Ag2S↓表示可溶性硫化物的盐类物质与硝酸银反应,故B不选;
C.CH3COOH在离子反应中保留化学式,则CO32-+2H+=H2O+CO2↑表示可溶性碳酸盐与强酸反应,故C不选;
D.AgNO3+NaCl=NaNO3+AgCl↓的离子反应为Ag++Cl-=AgCl↓,故D选;
故选D.
点评 本题考查离子反应方程式的书写,为高频考点,把握离子反应的书写方法及意义为解答的关键,侧重复分解反应的离子反应考查,注意离子反应中保留化学式的物质,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 14g乙烯、丙烯、丁烯的混合气体中所含原子数为3NA | |
| B. | 28g乙烯所含共用电子对数目为5NA | |
| C. | 标准状况下,11.2 L氯仿所含分子数为0.5 NA | |
| D. | 46g乙醇中含有C-H键数目为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

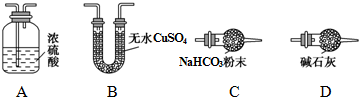
| 乙装置的质量(g) | 丙装置的质量(g) | |
| 加热前 | 80.00 | 62.00 |
| 加热后 | 80.36 | 62.88 |

查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 元素 | 结构或性质 |
| A | 原子最外层电子数是内层电子总数的$\frac{1}{5}$ |
| B | 形成化合物种类最多的元素,其单质为固体 |
| C | 生活中常见的金属,它有两种常见的氯化物,且相对分子质量相差35.5 |
| D | 地壳中含量最多的元素 |
| E | 与D同主族 |
| F | 与E同周期,且最外层电子数等于电子层数 |
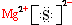 .
.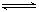 Al(OH)3
Al(OH)3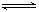 H++AlO2-+H2O;F的单质与C、D形成的相对分子质量为160的化合物在一定条件下反应的化学方程式是2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
H++AlO2-+H2O;F的单质与C、D形成的相对分子质量为160的化合物在一定条件下反应的化学方程式是2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烷和乙酸 | B. | 淀粉和纤维素 | ||
| C. | CH3CH2CH2CH3和CH3CH2CH3 | D. | 乙醇和二甲醚 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2:3 | B. | 1:3:2 | C. | 2:4:5 | D. | 2:3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .其反应类型为消去反应.检验生成的乙烯要将气体先后通入氢氧化钠溶液、酸性高锰酸钾溶液或溴水中.(填试剂名称)
.其反应类型为消去反应.检验生成的乙烯要将气体先后通入氢氧化钠溶液、酸性高锰酸钾溶液或溴水中.(填试剂名称)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | C | D | F | |||||
| 三 | B | E | G | R | ||||
| 四 | A | H |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
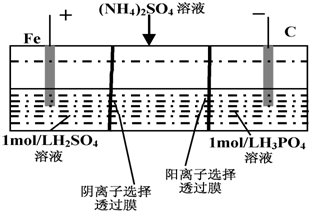
| A. | 阳极室溶液由无色变成棕黄色 | |
| B. | 阴极的电极反应式为:4OH--4e-=2H2O+O2↑ | |
| C. | 电解一段时间后,阴极室溶液中的酸性减弱 | |
| D. | 电解一段时间后,阴极室溶液中的溶质一定是(NH4)3PO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com