
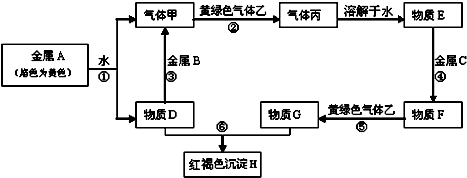
分析 金属单质A的焰色反应为黄色,应为Na,与水反应生成的气体甲为H2,D为NaOH,黄绿色气体乙为Cl2,则丙为HCl,E为盐酸,能与NaOH反应生成氢气的B为Al,红褐色沉淀H为Fe(OH)3,则C为Fe,F为FeCl2 ,G为FeCl3,结合对应物质的性质以及题目要求解答该题.
解答 解:金属单质A的焰色反应为黄色,应为Na,与水反应生成的气体甲为H2,D为NaOH,黄绿色气体乙为Cl2,则丙为HCl,E为盐酸,能与NaOH反应生成氢气的B为Al,红褐色沉淀H为Fe(OH)3,则C为Fe,F为FeCl2 ,G为FeCl3,
(1)由以上分析可知D为NaOH,乙为Cl2,
故答案为:NaOH;Cl2;
(2)①为钠与水的反应,生成氢氧化钠和氢气,反应的方程式为2Na+2H2O=2Na++2OH-+H2↑,
③为铝和氢氧化钠溶液生成氢气的反应,方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Na+2H2O=2Na++2OH-+H2↑;2Al+2OH-+2H2O=2AlO2-+3H2↑;
(3)氯化亚铁与氢氧化钠反应生成白色氢氧化亚铁沉淀,氢氧化亚铁不稳定,易被空气中氧气氧化生成氢氧化铁,可观察到白色沉淀逐渐变成灰绿色,最终变成红褐色,
反应的方程式为FeCl2+2NaOH=Fe(OH)2↓+2NaCl、4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:产生白色沉淀,逐渐变成灰绿色,最终变成红褐色;FeCl2+2NaOH=Fe(OH)2↓+2NaCl;4Fe(OH)2+O2+2H2O=4Fe(OH)3 .
点评 本题考查无机物的推断,侧重于学生的分析能力的考查,为高考常见题型,以无机框图题的形式考查Na、Al、Fe、Cl等元素单质及其化合物之间的相互转化关系,以“焰色反应、黄绿色气体、红褐色沉淀”为突破口采用正逆结合的方法进行推断,难度中等,注意基础知识的掌握.


科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•Lˉ1BaCl2溶液 | B. | 澄清石灰水 | ||
| C. | 稀盐酸 | D. | pH试纸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用饱和Na2CO3溶液除去混在CO2中的HCl气体 | |
| B. | 用Cl2除去Fe2(SO4)3溶液中的少量FeSO4 | |
| C. | 用加热的方法除去混在碳酸钠固体中的碳酸氢钠杂质 | |
| D. | 向AlCl3溶液中加入过量的NaOH溶液以制备Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发操作时,应使蒸发皿中的水分完全蒸干后,才能停止加热 | |
| B. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| C. | 除去铜粉中混有的少量镁粉和铝粉可加入足量氢氧化钠溶液,反应后过滤、洗涤 | |
| D. | 加入盐酸,放出无色气体,该气体能使澄清石灰水变浑浊的气体,则原溶液中有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色黏稠液体,易溶于水.为研究A的组成与结构,进行了如下实验:
有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色黏稠液体,易溶于水.为研究A的组成与结构,进行了如下实验: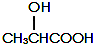 .A与浓H2SO4混合,在一定条件下反应生成六元环状物B,B的结构简式
.A与浓H2SO4混合,在一定条件下反应生成六元环状物B,B的结构简式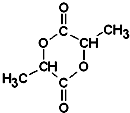 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
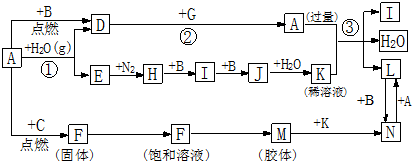
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.012 kg 12C中含有约6.02×1023个碳原子 | |
| B. | 1 mol H2O中含有2 mol氢和1 mol氧 | |
| C. | 物质的量就是1 mol物质的质量 | |
| D. | 2 mol水的摩尔质量是1 mol水的摩尔质量的2倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| A | 盐酸 | 水煤气 | 硫酸 | 醋酸 | HD |
| B | 胆矾 | 石灰水 | 硫酸钡 | HNO2 | NH3 |
| C | 火碱 | 蔗糖溶液 | 氯化钠 | 氨水 | 三氧化硫 |
| D | 冰醋酸 | 福尔马林 | 苛性钾 | 碘化氢 | 乙醇 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com