
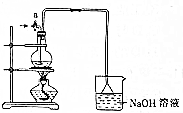
 某化学探究小组为探究能与碳反应的浓硫酸的最低浓度,设计了如图实验装置进行实验.
某化学探究小组为探究能与碳反应的浓硫酸的最低浓度,设计了如图实验装置进行实验.分析 有活塞或连接仪器的装置实验前必须检验装置气密性,加热条件下碳和浓硫酸发生C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,因二氧化硫、二氧化碳与氢氧化钠反应,为防止倒吸,吸收装置利用倒扣漏斗而不是将导管直接插入溶液,装置中长导气管兼起导气冷凝的作用,使水蒸气冷凝回流,起到了确保硫酸溶液体积保持不变的作用,以此解答该题.
解答 解:(1)实验装置是制备二氧化硫气体的发生装置,在实验前需要检验装置气密性,防止装置漏气影响实验,故答案为:检验装置气密性;
(2)加热条件下碳和浓硫酸发生C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,故答案为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;
(3)反应生成二氧化碳、二氧化硫,可与氢氧化钠溶液反应而被吸收,利用倒置的漏斗而不是将导气管直接伸入烧杯中是防止液体倒吸,故答案为:CO2、SO2;防倒吸;
(4)由导管a通入足量的空气,以确保烧瓶中的SO2气体全部进入烧杯中,装置中长导气管兼起导气冷凝的作用,使水蒸气冷凝回流,起到了确保硫酸溶液体积保持不变的作用,
故答案为:SO2气体全部进入烧杯中;冷凝回流;
(5)加入硝酸把亚硫酸钠氧化为硫酸钠,加入氯化钡溶液反应生成硫酸钡沉淀,通过过滤、洗涤、干燥得到沉淀,称量固体的质量为27.96g为硫酸钡沉淀,物质的量=$\frac{27.96g}{233g/mol}$=0.12mol,依据硫元素守恒,被氧化的硫酸为0.12mol,依据化学方程式可知,C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,反应的硫酸物质的量为0.24mol,剩余硫酸物质的量=18mol/L×0.020L-0.24mol=0.12mol,需要的最低浓度=$\frac{0.12mool}{0.02L}$=6mol/L,
故答案为:过滤、洗涤、干燥;6mol/L.
点评 本题以浓硫酸和Cu的反应为载体考查性质实验方案设计,为高频考点,涉及基本计算、基本操作、氧化还原反应等知识点,明确实验基本操作、物质性质是解本题关键,注意实验的评价,难点是(5)题分析解答.


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:解答题
| 物理性质 | 制备原理 | 化学性质 |
| 黄色油状液体,熔点为-40℃,沸点为71℃,不溶于冷水,易溶于有机溶剂,密度为1.65g/mL | Cl2与NH4Cl水溶液在低温下反应 | 95℃爆炸,热水中发生水解 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 47.87是丰度最高的钛原子的相对原子质量 | |
| B. | 钛原子的M层上共有10个电子 | |
| C. | 从价电子构型看,钛属于某主族元素 | |
| D. | 22为钛原子的质量数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含大量Al3+的溶液中:K+、Na+、NO3-、CO32-不能大量共存,因有Al2(CO3)3沉淀生成 | |
| B. | 含大量Fe3+的溶液中:K+Mg2+、I-、Br2-不能大量共存,因2Fe3++2I-=2Fe2++I2 | |
| C. | 由水电离的c(H+)=1×10-14mol/L的溶液中:Ca2+、NO3-、HCO3-、Cl-不能大量共存,因溶液呈酸性,与HCO3-反应产生CO2气体 | |
| D. | 在NH4Fe(SO4)2溶液中:Na+、K+、S2-、SCN-不能大量共存,只是因Fe3+和S2-反应产生淡黄色的S沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向MgCl2溶液中加入过量的NaOH溶液,Mg2+沉淀完全,则溶液中不含Mg2+ | |
| B. | Ksp小的物质其溶解能力一定比Ksp大的物质的溶解能力小 | |
| C. | 25℃时,由于Kw(ZnS)>Kw(CuS),所以ZnS在一定条件下可转化为CuS | |
| D. | 0.1molAgCl和0.1molAgI混合后加入1L水中,所得溶液中c(Cl-)=c(I-) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
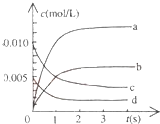 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑦ | B. | ②⑤⑥ | C. | ①④ | D. | ②③⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com