
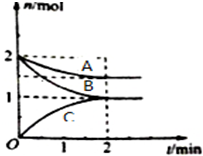
 Ņ»¶ØĪĀ¶ČĻĀ£¬Ä³ČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÄŚ£¬Ä³Ņ»·“Ó¦ÖŠA”¢B”¢CČżÖÖĘųĢåµÄĪļÖŹµÄĮæĖę·“Ó¦Ź±¼ä±ä»ÆµÄĒśĻßČēĶ¼ĖłŹ¾£ŗ
Ņ»¶ØĪĀ¶ČĻĀ£¬Ä³ČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÄŚ£¬Ä³Ņ»·“Ó¦ÖŠA”¢B”¢CČżÖÖĘųĢåµÄĪļÖŹµÄĮæĖę·“Ó¦Ź±¼ä±ä»ÆµÄĒśĻßČēĶ¼ĖłŹ¾£ŗ·ÖĪö £Ø1£©»Æѧ·“Ó¦ÖŠ£¬ø÷ĪļÖŹµÄĪļÖŹµÄĮæµÄ±ä»ÆÖµÓė»Æѧ¼ĘĮæŹż³ŹÕż±Č£¬ŅŌ“ĖŹéŠ“»Æѧ·½³ĢŹ½£»
£Ø2£©·“Ó¦ĖŁĀŹv=$\frac{”÷c}{”÷t}$£»
£Ø3£©·“Ó¦“ļµ½×ī“óĻŽ¶ČŹĒÖø·“Ó¦ŌŚŅ»¶ØĢõ¼žĻĀ“ļµ½Ę½ŗāדĢ¬£¬ÕżÄę·“Ó¦ĖŁĀŹĻąĶ¬£¬ø÷×é·Öŗ¬Įæ±£³Ö²»±ä£»
£Ø4£©Ōö“ó·“Ó¦ĖŁĀŹæÉŌö“óŃ¹Ēæ”¢ÉżøßĪĀ¶Č”¢ĢįøßÅضČŅŌ¼°Ź¹ÓĆ“ß»Æ¼ĮµČ£¬øł¾ŻĶā½ēĢõ¼ž¶Ō»Æѧ·“Ó¦ĖŁĀŹµÄÓ°Ļģ½ā“š£¬Ōö“óÅØ¶Č”¢Ń¹Ē攢ĪĀ¶Č”¢Õż“߻ƼĮ¾łæɼÓæģ·“Ó¦ĖŁĀŹ£¬µ«Ń¹ĒæÖ»Ó°ĻģÓŠĘųĢå²Ī¼ÓµÄ·“Ó¦£®
½ā“š ½ā£ŗ£Ø1£©Ķ¼Ļó·ÖĪöæÉÖŖ£¬2minAĪļÖŹµÄĮæ¼õÉŁ0.5mol£¬BĪļÖŹµÄĮæ¼õÉŁ1mol£¬CĪļÖŹµÄĮæŌö¼Ó1mol£¬ABĪŖ·“Ó¦Īļ£¬CĪŖÉś³ÉĪļ£¬·“Ó¦ĪļÖŹµÄĮæÖ®±ČµČÓŚn£ØA£©£ŗn£ØB£©£ŗn£ØC£©=0.5£ŗ1£ŗ1=1£ŗ2£ŗ2£®·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗA+2B?2C£¬
¹Ź“š°øĪŖ£ŗA+2B?2C£»
£Ø2£©Ķ¼Ļó·ÖĪöæÉÖŖ£¬·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬2minAĪļÖŹµÄĮæ¼õÉŁ0.5mol£¬·“Ó¦ĖŁĀŹv=$\frac{\frac{0.5mol}{2L}}{2min}$=0.125mol•L-1•min-1 £¬
¹Ź“š°øĪŖ£ŗ0.125mol•L-1•min-1 £»
£Ø3£©A£®·“Ó¦Ē°ŗóĘųĢåÖŹĮæ²»±ä£¬Ģå»ż²»±ä£¬»ģŗĻĘųĢåµÄĆÜ¶Č²»Ėꏱ¼äµÄ±ä»Æ¶ų±ä»Æ£¬²»ÄÜĖµĆ÷·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬¹ŹA“ķĪó£»
B£®·“Ó¦Ē°ŗóĘųĢåĪļÖŹµÄĮæ±ä»Æ£¬ĘųĢåŃ¹Ēæøı䣬µ±»ģŗĻĘųĢåµÄŃ¹Ēæ²»Ėꏱ¼äµÄ±ä»Æ¶ų±ä»ÆĖµĆ÷·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬¹ŹBÕżČ·£»
C£® »Æѧ·½³ĢŹ½¼ĘĮæŹżÖ®±ČĖŁĀŹÖ®±Č£¬V£ØA£©£ŗV£ØB£©=1£ŗ2£¬²»ÄÜĖµĆ÷·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬¹ŹC“ķĪó£»
¹Ź“š°øĪŖ£ŗB£»
£Ø4£©A£®ÉżĪĀæÉŌö“ó·“Ó¦ĖŁĀŹ£¬¹ŹAŃ”£»
B£®Ōö“óČŻĘ÷µÄĢå»ż£¬Ń¹Ēæ¼õŠ”·“Ó¦ĖŁĀŹ¼õŠ”£¬¹ŹB²»Ń”£»
C£®¼õŠ”AµÄÅØ¶Č£¬·“Ó¦ĖŁĀŹ¼õŠ”£¬¹ŹC²»Ń”£»
D£®³äČė¶čŠŌĘųĢåŹ¹½«·“ӦȯĘ÷ÄŚŃ¹ĒæŌö“󣬵«ĘųĢå·ÖŃ¹²»±ä£¬Ę½ŗā²»±ä£¬·“Ó¦ĖŁĀŹ²»±ä£¬¹ŹD²»Ń”£®
¹Ź“š°øĪŖ£ŗA£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»Æѧ·“Ó¦ĖŁĀŹøÅÄī”¢Ķ¼Ļó·ÖĪöÅŠ¶Ļ”¢Ó°Ļģ»Æѧ·“Ó¦ĖŁĀŹŗĶ»ÆŃ§Ę½ŗāµÄŅņĖŲµČÖŖŹ¶µć£¬ÕĘĪÕ»ł“”ŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaOH¹ĢĢåÖŠÖ»ŗ¬Ąė×Ó¼ü | |
| B£® | XµÄĘųĢ¬Ēā»ÆĪļµÄ»ÆѧŹ½ĪŖH2X£¬ŌņXµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄ»ÆѧŹ½ĪŖH3XO4 | |
| C£® | HClµÄŠĪ³É¹ż³ĢÓƵē×ÓŹ½±ķŹ¾ĪŖ | |
| D£® | ĀĮÓėĻ”ŃĪĖįµÄ·“Ó¦¼ČŹĒŃõ»Æ»¹Ō·“Ó¦£¬ÓÖŹĒ·ÅČČ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
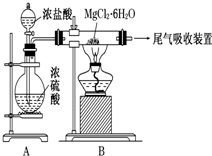
| A£® | Ī²ĘųĪüŹÕæÉŅŌÓĆÅØĮņĖį×÷ĪŖĪüŹÕ¼Į½ųŠŠĪüŹÕ | |
| B£® | ×°ÖĆAÖŠŌ²µ×ÉÕĘæÖŠæÉŅŌ»»³É¹ĢĢåMnO2 | |
| C£® | Čē¹ūÖ±½Ó¼ÓČČMgCl2•6H2O²»ÄܵƵ½ĪŽĖ®ĀČ»ÆĆ¾£¬½«æÉÄܵƵ½MgO | |
| D£® | ½šŹōĆ¾ŌŚæÕĘųÖŠČ¼ÉÕ£¬¾ēĮŅ·“Ӧɜ³ÉŃõ»ÆĆ¾£¬Čē¹ū½šŹōĆ¾Č¼ÉÕ·¢Éś»šŌÖ£¬ŅŖĮ¢¼“ÓƶžŃõ»ÆĢ¼Ćš»šĘ÷½ųŠŠĆš»š |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µ„Ī»Ź±¼äÄŚĻūŗÄamol H2£¬Ķ¬Ź±ĻūŗÄ 2amol HI | |
| B£® | ČŻĘ÷ÄŚµÄ×ÜŃ¹Ēæ²»Ėꏱ¼ä±ä»Æ | |
| C£® | ČŻĘ÷ÄŚH2”¢I2²»ŌŁ¼õÉŁ£¬HI²»ŌŁŌö¼Ó | |
| D£® | µ„Ī»Ź±¼äÄŚĆæÉś³Éamol HI£¬Ķ¬Ź±a NAøöHI·Ö×Ó·Ö½ā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH3-CHØTCH2 | B£® | CH3-CH2-CHØTCH2 | C£® |  | D£® | CH2ØTCH-CHØTCH2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČ»ÆĢśČÜŅŗÖŠ¼ÓÉŁĮæĮņĒč»Æ¼ŲČÜŅŗ£ŗFe3++3SCN-ØTFe£ØSCN£©3”ż | |
| B£® | ĮņĖįĶČÜŅŗÖŠ¼Ó¹żĮæ°±Ė®£ŗCu2++2NH3•H2OØTCu£ØOH£©2”ż+2NH4+ | |
| C£® | µā»Æ¼ŲČÜŅŗÖŠ¼Ó¹żĮæĀČĖ®£ŗ2I-+Cl2ØTI2+2Cl- | |
| D£® | ±½·ÓÄĘČÜŅŗÖŠĶØÉŁĮæCO2£ŗ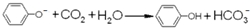 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
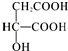 £¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | Ę»¹ūĖįÖŠÄÜ·¢Éśõ„»Æ·“Ó¦µÄ¹ŁÄÜĶÅÓŠ2ÖÖ | |
| B£® | 1 molĘ»¹ūĖįæÉÓė3 mol NaOH·¢ÉśÖŠŗĶ·“Ó¦ | |
| C£® | 1 molĘ»¹ūĖįÓė×ćĮ潚ŹōNa·“Ӧɜ³É1 mol H2 | |
| D£® | 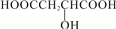 ÓėĘ»¹ūĖį»„ĪŖĶ¬·ÖŅģ¹¹Ģå ÓėĘ»¹ūĖį»„ĪŖĶ¬·ÖŅģ¹¹Ģå |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com