
分析 (1)坩埚灼烧晶体的装置和操作选择需要的仪器;
(2)亚硫酸钠具有强的还原性,易被氧气氧化为硫酸钠;
(3)Na2SO3在高温强热下发生分解反应是一个自身氧化还原反应,会生成低价硫和高价硫;
(4)硫离子和亚硫酸根离子均能发生水解使得溶液显碱性,水解程度不一样而碱性强弱不一样;
(5)根据硫离子能和酸反应生成硫化氢、硫酸根离子可以和钡离子反应生成硫酸钡来回答.
解答 解:(1)实验操作②中除坩埚、酒精灯、三角架及隔绝空气的设备外,还需要的仪器有泥三角、坩埚钳,
故答案为:泥三角、坩埚钳;
(2)亚硫酸钠具有强的还原性,Na2SO3•7H2O加热时要隔绝空气,防止亚硫酸钠被氧气氧化为硫酸钠,即2Na2SO3+O2=2Na2SO4;
故答案为:避免Na2SO3被空气中氧气氧化,2Na2SO3+O2=2Na2SO4;
(3)Na2SO3在高温强热下发生分解反应是一个自身氧化还原反应,会生成-2价硫和+6价的硫,反应为:4Na2SO3$\frac{\underline{\;高温\;}}{\;}$Na2S+3Na2SO4,
故答案为:4Na2SO3$\frac{\underline{\;高温\;}}{\;}$Na2S+3Na2SO4;
(4)硫离子和亚硫酸根离子均能发生水解使得溶液显碱性,实验①和③中,两次测得的溶液pH相差明显,是因为二者的水解程度不一样而导致碱性强弱不一样,实验③中溶液的pH=10.3的原理是S2-+H2O?HS-+OH-,
故答案为:实验③的溶液中可能有Na2S,相同条件下,S2-水解程度大于SO32-,溶液的碱性强;S2-+H2O?HS-+OH-;
(5)硫离子能和酸反应生成硫化氢,硫离子的检验方法:取③溶液适量于试管中,向其中加稀H2SO4,如有腐蛋气味气体生成,则证明有S2-,硫酸根离子可以和钡离子反应生成硫酸钡,硫酸根离子的检验方法:另取③中溶液适量于试管中,加入HCl酸化的BaCl2,如有白色沉淀生成,证明有SO42-,
故答案为:取③溶液适量于试管中,向其中加稀H2SO4,如有腐蛋气味气体生成,则证明有S2-;另取③中溶液适量于试管中,加入HCl酸化的BaCl2,如有白色沉淀生成,证明有SO42-.
点评 本题是一道信息迁移题,考查学生对知识的综合程度和解决问题的能力,难度中等.充分利用题给信息“①常温下0.1mol•L-1的H2SO3溶液的pH约为2.1.②通常情况下,H2S为无色,有腐蛋臭味的气体,其水溶液称为氢硫酸.常温下0.1mol•L-1的H2S溶液的pH约为4.5及Na2SO3•7H2O在强热下,失去结晶水,进而发生了分解反应(自身氧化还原反应)”是解题关键.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| 元素 | I1 | I2 | I3 | I4 |
| X | 500 | 4600 | 6900 | 9500 |
| Y | 580 | 1800 | 2700 | 11600 |
| A. | 元素X的常见化合价是+1价 | |
| B. | 元素Y是IIIA族元素 | |
| C. | 若元素Y处于第3周期,它的单质可与冷水剧烈反应 | |
| D. | 元素X与氯元素形成化合物时,化学式可能是XCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
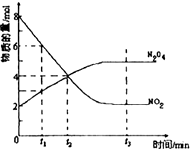 一定温度下,在容积为1L的密闭容器中放入2molN2O4和8molNO2,发生如下反应2NO2(红棕色)═N2O4(无色)△H<0反应中NO2、N2O4的物质的量随反应时间变化的曲线如图,按下列要求作答:
一定温度下,在容积为1L的密闭容器中放入2molN2O4和8molNO2,发生如下反应2NO2(红棕色)═N2O4(无色)△H<0反应中NO2、N2O4的物质的量随反应时间变化的曲线如图,按下列要求作答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2P2(g)═P4(g)△H=-229.7 kJ•mol-1 | B. | P2制P4是放热反应 | ||
| C. | P2比P4更加稳定 | D. | 等质量时,P2比P4具有的能量高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2+、Na+、NO3-、Cl- | B. | Mg2+、NH4+、SO42-、NO3- | ||
| C. | H+、K+、Cl-、CH3COO- | D. | K+、Mg2+、CO32-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ/mol | |
| B. | 已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3 kJ/mol,则含0.5 mol NaOH的稀溶液与稀醋酸完全中和,放出的热量小于28.65kJ | |
| C. | 可燃物的系数为1的燃烧反应的焓变即为该可燃物的燃烧热 | |
| D. | 已知2C(s)+2O2(g)═2CO2(g)△H=a kJ/mol,2C(s)+O2(g)═2CO(g)△H=b kJ/mol,则a>b |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. 两边基团换位的反应.如两个丙烯分子进行烯烃换位,生成丁烯和乙烯.
两边基团换位的反应.如两个丙烯分子进行烯烃换位,生成丁烯和乙烯. +H2O
+H2O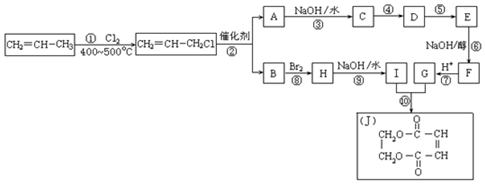
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com