
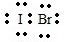 ,它是由极性共价键形成的极性分子.
,它是由极性共价键形成的极性分子.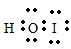 .
.分析 (1)I和Br的电负性相差不大,形成的化学键是极性共价键,根据共价化合物的成键特点书写电子式;
(2)溴化碘(IBr)的化学性质类似于卤素单质,得知溴化碘和水反应生成次碘酸和溴化氢,结合HClO书写HIO的电子式;
(3)Br为第四周期元素,最外层电子数为7.
解答 解:(1)I和Br的电负性相差不大,形成的化学键是极性共价键,电子式为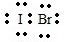 ,是极性共价键形成的极性分子,
,是极性共价键形成的极性分子,
故答案为: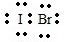 ;极性共价;极性.
;极性共价;极性.
(2)根据卤素单质和水之间反应生成次卤酸和卤化氢,由于Br比I的电负性大,溴化碘和水反应生成次碘酸和溴化氢,三原子分子为次碘酸,属于共价化合物,电子式为: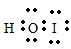 ,故答案为:
,故答案为: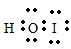 ;
;
(3)Br为第四周期元素,最外层电子数为7,则溴的价电子排布式为4s24p5,故答案为:4s24p5.
点评 本题考查IBr的结构,为高频考点,把握卤素元素及化合物结构与性质的相似性为解答的关键,侧重分析与迁移应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 当12NA个电子转移时,该反应放出1411 kJ的能量 | |
| B. | 当2NA个水分子生成且为液体时,放出1411 kJ的能量 | |
| C. | 当8NA个碳氧共用电子对生成时,放出1411 kJ的能量 | |
| D. | 当8NA个碳氧双键生成时,放出1411 kJ的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化碳分子的结构式:O-C-O | |
| B. | 氢氧根离子的电子式: | |
| C. | 氯原子的结构示意图: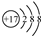 | |
| D. | 中子数为146、质子数为92 的铀(U)原子${\;}_{92}^{146}$U |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ②③ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
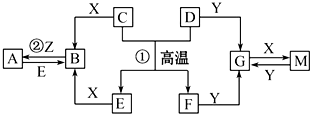
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
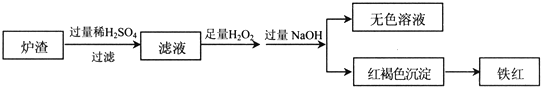
| 实验方案 | 预期现象 | |
| a | 加NaOH溶液 | 产生白色沉淀,变灰绿再变红褐 |
| b | 先加KSCN溶液,再加氯水 | 先无明显现象,后变红 |
| C | 加酸性KMnO4溶液 | 紫色褪去 |
| d | 先加氯水,再加KSCN溶液 | 溶液先变黄,再变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的标准燃烧热为890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为: N2(g)+3H2(g) $?_{500℃、30MPa}^{催化剂}$ 2NH3(g)△H=-38.6 kJ•mol-1 | |
| C. | 相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量 | |
| D. | 1 mol NaOH分别和1 mol CH3COOH、1 mol HNO3反应,后者比前者放出的热量多 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/g/L | 63.7 | 28.8 | 144.6 | 46.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
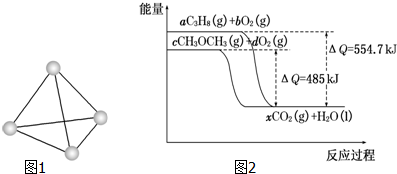
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com