
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2015-2016学年山东省临沂市高一上学期第一次月考化学试卷(解析版) 题型:选择题
下列判断正确的是
A.1 L H2O中溶解了0.5 mol NaCl,则该溶液的物质的量浓度为0.5 mol·L-1
B.从1 L 1 mol·L-1蔗糖(C12H22O11)溶液中取出100 mL溶液,其物质的量的浓度仍为1 mol·L-1
C.0.5 mol·L-1的NaOH溶液中,含有0.5 mol Na+
D.1 L H2SO4溶液中含有98 g H2SO4,则该溶液的物质的量浓度为98 g·L-1
查看答案和解析>>
科目:高中化学 来源:2016届江西省红色七校高三上学期第一次联考化学试卷(解析版) 题型:填空题
(10分)纯过氧化氢是淡蓝色的黏稠液体,可任意比例与水混合,是一种强氧化剂,水溶液俗称双氧水,为无色透明液体。其水溶液适用于医用伤口消毒及环境消毒和食品消毒。
(1)请写出H2O2的电子式 。
(2)往硫酸中加入一定浓度的双氧水可将溶解铜,写出该反应的离子方程式_________________。
(3)Fe3+催化H2O2分解的机理可分两步反应进行,第一步反应为:2Fe3++H2O2=2Fe2++O2↑+2H+,
请完成第二步反应的离子方程式:
 Fe2++
Fe2++  H2O2 +
H2O2 +  _________ ==
_________ ==  _________+
_________+  _________
_________
(4)下图是一种用电解原理来制备过氧化氢并用产生的H2O2处理废氨水的装置
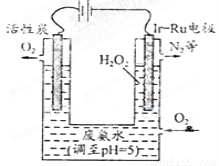
①为了不影响H2O2的产量,需要向废氨水加入适量硝酸调节溶液的pH约为5,则所得废氨水溶液中c(NH4+)____ c(NO3-)(填“>”、“<”或“=”)。
②Ir-Ru惰性电极有吸附O2作用,该电极上的反应为 。
③理论上电路中每转移3mol电子,最多可以处理NH3·H2O的物质的量为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省临沂市高二上10月月考化学试卷(解析版) 题型:选择题
在一个体积固定的密闭容器中加入2 mol A和1 mol B,发生反应:2A(g)+B(g)?3C(g)+D(g),达到平衡时C的浓度为a mol/L.若维持容器体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍为a mol/L的是
A.4mol A+2mol B
B.2mol A+1mol B+3mol C+1mol D
C.3mol C+1mol D+1mol B
D.3mol C+1mol D
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西大学附属中学高一上学期第一次月考化学试卷(解析版) 题型:选择题
在标准状况下,由CO和CO2组成的混合气体13.44 L,质量为24克,此混合气体中C和O两种原子的物质的量之比是
A.2∶7 B.3∶7 C.4∶7 D.5∶7
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二上学期第一次月考化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.在化学反应进行的过程中放出或吸收的热量称为反应热
B.在稀溶液中,1mol酸跟1mol碱发生中和反应所放出的热量叫做中和热
C.对于吸热反应,反应物所具有的总能量总是低于生成物所具有的总能量
D.在101Kpa时,1mol物质完全燃烧生成稳定氧化物时,所放出的热量叫做该物质的燃烧热
查看答案和解析>>
科目:高中化学 来源:2016届江苏省淮安市高三上学期9月月考化学试卷(解析版) 题型:选择题
在下列溶液中,各组离子一定能够大量共存的是
A.水电离的c(H+)=10-12 mol·L-1的溶液:K+、Ba2+、Cl-、Br-
B.使酚酞试液变红的溶液:Na+、Cl-、SO42-、Fe3+
C.使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl-
D.含碳酸氢钠的溶液:K+、SO42-、Cl-、H+
查看答案和解析>>
科目:高中化学 来源:2016届湖南省常德市高三上学期10月月考化学试卷(解析版) 题型:推断题
(12分)邻羟基桂皮酸是合成香精的重要原料,下为合成邻羟基桂皮酸的路线之一

 已知:
已知:
试回答下列问题:
(1)化合物II的结构简式为:________________________
(2)化合物II→化合物III的有机反应类型________________
(3)化合物III在银氨溶液中发生反应化学方程式___________________
(4)有机物X为化合物IV的同分异构体,且知有机物X有如下特点:①是苯的对位取代物,②能与NaHCO3反应放出气体,③能发生银镜反应。请写出化合物X的结构简式_____________________
(5)下列说法正确的是
A.化合物I遇氯化铁溶液呈紫色
B.化合物II能与NaHCO3溶液反应
C.1mol化合物IV完全燃烧消耗9.5molO2
D.1mol化合物III能与3molH2反应
(6)有机物R(C9H9ClO3)经过反应、再酸化也可制得化合物IV,则R在NaOH醇溶液中反应的化学方程式为。
查看答案和解析>>
科目:高中化学 来源:2016届安徽省安庆市高三上学期第一次质检化学试卷(解析版) 题型:实验题
(10分)(a)铁元素在人类生活中扮演着非常重要的角色,不仅仅是重要的建筑材料,也是人体必须的微量元素。每年钢铁的腐蚀带来巨大的经济损失。某校研究小组在实验室中模拟钢铁在自然环境下的腐蚀,设置如下装置,几天后观察结果:
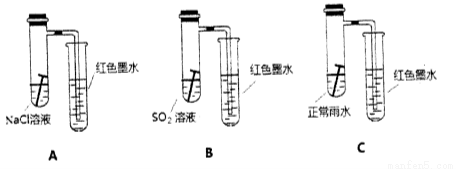
请回答下列问题:
(1)请比较以上三个装置中右侧导管中红墨水的高度: > > 。请写出A装置中,钢铁锈蚀时正极反应的电极反应式 。
(2)钢铁的防腐有重大的意义,生活中常将金属制品放在干燥处或者涂上矿物油予以保护,现请你从电化学角度设计一种方法保护下图中钢铁以免被腐蚀,请将下图完成:
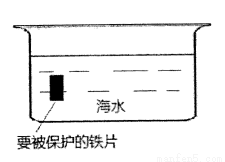
(b)下面是一种常见补铁药品说明书中的部分内容:该药品含Fe2+:33%~36%,不溶于水但能溶于人体中的胃酸,与Vc(维生素C)同服可增加本品吸收。某乙同学采用在酸性条件下用高锰酸钾标准溶液滴定的方法测定该药品是否合格,反应原理为:
5 Fe2++8H++MnO4-=5 Fe3++Mn2++4H2O
准确称量上述药品10.00g,将其全部溶于试剂1中,配制成1000mL溶液,取出20.00mL,用0.0200mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL。
(3)该实验中的试剂1是 (填序号)。
A.蒸馏水 B.稀盐酸 C.稀硫酸 D.稀硝酸
(4)请简述判断滴定终点的现象: 。
(5)请通过计算,说明该药品含铁量是否合格 (填“合格”或“不合格”)(Fe的摩尔质量为56g/mol)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com