
| A£® | 4Na+O2ØT2Na2O | B£® | NH4HCO3ØTNH3”ü+H2O+CO2”ü | ||
| C£® | NH3+HClØTNH4C1 | D£® | H2SO4+2NaOHØTNa2SO4+2H2O |
·ÖĪö Ńõ»Æ»¹Ō·“Ó¦µÄŹµÖŹĪŖµē×Ó×ŖŅĘ”¢ĢŲÕ÷ĪŖ»ÆŗĻ¼ŪÉż½µ£¬ĖłŅŌŃõ»Æ»¹Ō·“Ó¦ÖŠŅ»¶Ø“ęŌŚŌŖĖŲ»ÆŗĻ¼Ū±ä»Æ£¬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗA£®Na”¢OŌŖĖŲ»ÆŗĻ¼Ū·¢Éś±ä»Æ£¬ŹōÓŚŃõ»Æ»¹Ō·“Ó¦£¬¹ŹAÕżČ·£»
B£®ĪŖ·Ö½ā·“Ó¦£¬·“Ó¦ÖŠ²»“ęŌŚ»ÆŗĻ¼Ū±ä»Æ£¬²»ŹōÓŚŃõ»Æ»¹Ō·“Ó¦£¬¹ŹB“ķĪó£»
C£®ĪŖ»ÆŗĻ·“Ó¦£¬·“Ó¦ÖŠ²»“ęŌŚ»ÆŗĻ¼Ū±ä»Æ£¬²»ŹōÓŚŃõ»Æ»¹Ō·“Ó¦£¬¹ŹC“ķĪó£»
D£®ĪŖÖŠŗĶ·“Ó¦£¬²»“ęŌŚ»ÆŗĻ¼Ū±ä»Æ£¬²»ŹōÓŚŃõ»Æ»¹Ō·“Ó¦£¬¹ŹD“ķĪó£®
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éĮĖŃõ»Æ»¹Ō·“Ó¦µÄÅŠ¶Ļ£¬ĢāÄæÄŃ¶Č²»“ó£¬Ć÷Č·Ńõ»Æ»¹Ō·“Ó¦µÄŹµÖŹ”¢ĢŲÕ÷ĪŖ½ā“š¹Ų¼ü£¬×¢ŅāÕĘĪÕĖÄÖÖ»ł±¾·“Ó¦ĄąŠĶÓėŃõ»Æ»¹Ō·“Ó¦Ö®¼äµÄ¹ŲĻµ£¬ŹŌĢāÓŠĄūÓŚĢįøßѧɜµÄĮé»īÓ¦ÓĆÄÜĮ¦£®


 ÓżӾ«¾ķĻµĮŠ“š°ø
ÓżӾ«¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
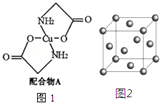 ŅŃÖŖ£ŗĮņĖįĶČÜŅŗÖŠµĪČė°±»łŅŅĖįÄĘ£ØH2N-CH2-COONa£©¼“æɵƵ½ÅäŗĻĪļA£®Ęä½į¹¹ČēĶ¼1ĖłŹ¾
ŅŃÖŖ£ŗĮņĖįĶČÜŅŗÖŠµĪČė°±»łŅŅĖįÄĘ£ØH2N-CH2-COONa£©¼“æɵƵ½ÅäŗĻĪļA£®Ęä½į¹¹ČēĶ¼1ĖłŹ¾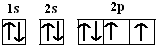 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | pH=1µÄČÜŅŗÖŠ£ŗNa+”¢K+”¢MnO4-”¢CO32- | |
| B£® | c£ØH+£©=1”Į10-13mol/LµÄČÜŅŗÖŠ£ŗK+”¢Na+”¢NO3-”¢CH3COO- | |
| C£® | 0.1mol•L-1NH4HCO3ČÜŅŗ£ŗNa+”¢Fe3+”¢NO3-”¢Cl- | |
| D£® | 0.1mol•L-1FeCl3ČÜŅŗ£ŗFe2+”¢NH4+”¢SCN-”¢SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÉśŹÆ»Ņ | B£® | ľĢæ | C£® | ĮņĖį±µ | D£® | ĀČ»ÆÄĘ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | 1 molƧ²ŻĖįĶźČ«Č¼ÉÕĻūŗÄ156.8 L O2 | |
| B£® | 1 molƧ²ŻĖį×ī¶ąÓė4 mol Na·¢Éś·“Ó¦ | |
| C£® | Ƨ²ŻĖįÄÜŹ¹äåµÄĖÄĀČ»ÆĢ¼ČÜŅŗĶŹÉ« | |
| D£® | Ƨ²ŻĖįæÉ·¢Éś¾ŪŗĻ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ńõ»ÆĪļ”¢Ēā»ÆĪļ¶¼ŹĒÖ»ŗ¬¶žÖÖŌŖĖŲ | |
| B£® | »ģŗĻĪļÖŠµÄŌŖĖŲŅ»¶ØŹĒ»ÆŗĻĢ¬µÄŠĪŹ½“ęŌŚ | |
| C£® | ½šŹōŃõ»ÆĪļŅ»¶ØŹĒ¼īŠŌŃõ»ÆĪļ | |
| D£® | ÓÉŅ»ÖÖŌŖĖŲ×é³ÉµÄĪļÖŹŅ»¶ØŹĒ“æ¾»Īļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com