
| A. | Na2S | B. | Na3PO4 | C. | Na2CO3 | D. | AlCl3 |
分析 根据盐类的电离和水解判断所含粒子的种类,得出正确结论,注意多元弱酸分步水解,水溶液中存在水的电离平衡.
解答 解:A、Na2S溶液中,有钠离子、氢离子、硫氢根离子、硫离子、氢氧根离子,共5种离子;
B、Na3PO4溶液中,PO43-要水解,所含粒子为Na+、PO43-、HPO42-、H2PO4-、H3PO4、H2O、H+、OH-,共8种粒子;
C、Na2CO3溶液中,有钠离子、氢离子和碳酸氢根离子,碳酸根离子和氢氧根离子,共5种;
D、AlCl3溶液中,有铝离子、氢离子、氯离子和氢氧根离子;共4种;
故含粒子种类(分子和离子)最多的是Na3PO4溶液,
故选:B.
点评 本题主要考查了溶液中微粒种类,主要从盐类电离、水解以及水的电离进行思考,题目难度不大


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 仪器 | 试剂 | 实验目的 |
| A | 托盘天平(带砝码)、滴管、量筒、烧杯、药匙、玻璃棒 | 食盐,蒸馏水 | 配制一定物质的量浓度的NaCl溶液 |
| B | 烧杯、漏斗、滴管、铁架台(带铁圈)、玻璃棒、滤纸、导气管 | 烧碱,CO2,稀盐酸 | 除去AlCl3溶液中少量的MgCl2 |
| C | 酸式滴定管、滴管、铁架台(带铁夹) | 已知浓度的盐酸、石蕊 | 测定NaOH溶液的浓度 |
| D | 分液漏斗、烧瓶、锥形瓶、导管、橡皮塞 | 稀盐酸,大理石,硅酸钠溶液 | 证明非金属性:Cl> C>Si |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  表示25℃时,用0.1 mol•L-1盐酸滴定20 mL 0.1 mol•L-1 NaOH溶液,溶液的pH随加入酸体积的变化 | |
| B. |  图中曲线表示反应2SO2 (g)+O2 (g)?2SO3(g);△H<0 正、逆反应的平衡常数K随温度的变化 | |
| C. |  表示10 mL 0.01 mol•L-1KMnO4 酸性溶液与过量的0.1 mol•L-1H2 C2 O4溶液混合时,n(Mn2+) 随时间的变化 | |
| D. | 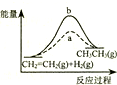 图中a、b曲线分别表示反应CH2=CH2 (g)+H2 (g)→CH3CH3(g);△H<0使用和未使用催化剂时,反应过程中的能量变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 肯定有KNO3 | B. | 肯定没有Ba(NO3)2,可能含有KNO3 | ||
| C. | 肯定没有Ba(NO3)2和Na2CO3 | D. | 肯定有KNO3,可能还含有Na2CO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com