
| A、K+NH4+Cl-NO3- |
| B、Cu2+H+HCO3-Cl- |
| C、Fe3+H+Cl-SCN- |
| D、Ba2+H+NO3-Fe2+ |


科目:高中化学 来源: 题型:
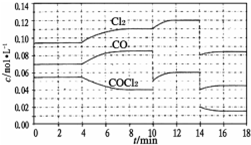 COCl2的分解反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如下图所示(第10min到14min的COCl2浓度变化曲线未示出).下列有关说法不正确的是( )
COCl2的分解反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如下图所示(第10min到14min的COCl2浓度变化曲线未示出).下列有关说法不正确的是( )| A、分解反应方程式为COCl2=Cl2+CO |
| B、第2min反应温度高于第8min反应温度 |
| C、在第8min反应温度下,12min时反应重新达到平衡,则此时c(COCl2)≈0.031mol/L |
| D、产物CO在2~3min、5~6min和12~13min时平均反应速率为v(5~6)>v(12~13)=v(2~3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 加入物质 | 对v (H2)影响 | 对n(H2)的影响 |
| Na2CO3 固体 | ||
| K2SO4 溶液 | ||
| NaNO3 固体 | ||
| 通入一定量HCl气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 类别组合 | 酸性氧化物 | 碱性氧化物 | 电解质 | 强电解质 | 高分子物质 |
| A | CO2 | CuO | 氨气 | NH3?H2O | 葡萄糖 |
| B | SO3 | Na2O | 稀硫酸 | NaOH | 果糖 |
| C | SO2 | CaO | 冰醋酸 | KOH | 纤维素 |
| D | N2O5 | Na2O2 | α-丙氨酸 | Cu(OH)2 | 聚乙烯 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、最终溶液:c(Na+)=1.5mol/L |
| B、标准状况下,反应过程中得到6.72 L气体 |
| C、最终溶液:c(Na+)=c(Cl-) |
| D、最终得到7.8 g沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com