
【题目】在1L定容的密闭容器中,可以证明可逆反应N2+3H2![]() 2NH3已达到平衡状态的是
2NH3已达到平衡状态的是
A. c(N2):c(H2):c(NH3)=1:3:2
B. 一个N≡N 断裂的同时,有3个H-H生成
C. 其他条件不变时,混合气体的密度不再改变
D. v正(N2)═2 v逆(NH3)
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】向体积为2![]() 的容器中加入1
的容器中加入1![]() N2和6molH2进行可逆反应:N2(g)+3H2(g)
N2和6molH2进行可逆反应:N2(g)+3H2(g)![]() 2NH3(g),2
2NH3(g),2![]() 后测得N2的物质的量为0.6mol,则:
后测得N2的物质的量为0.6mol,则:
(1)2![]() 内,H2的物质的量减少了_______mol,NH3的物质量增加了______mol。
内,H2的物质的量减少了_______mol,NH3的物质量增加了______mol。
(2)若用N2的浓度变化来表示该反应的反应速率为__________mol/(L·min)。
(3)若用NH3的浓度变化来表示该反应的反应速率为_________ mol/(L·min)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羟胺(NH2OH)是一种还原剂,能将某些氧化剂还原。现用25.00 mL 0.049 mol·L-1羟胺的酸性溶液与足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+恰好与24.55 mL 0.020 mol·L-1酸性KMnO4溶液完全反应。已知(未配平):FeSO4+KMnO4+H2SO4 → Fe2(SO4)+K2SO4+MnSO4+H2O,则羟胺的氧化产物是
A. N2 B. N2O C. NO D. NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国预计在2020年前后建成自己的载人空间站。为了实现空间站的零排放,循环利用人体呼出的CO2并提供O2,我国科学家设计了一种装置(如下图),实现了“太阳能一电能一化学能”转化,总反应方程式为2CO2=2CO+O2 。关于该装置的下列说法正确的是

A.图中N型半导体为正极,P型半导体为负极
B.图中离子交换膜为阳离子交换膜
C.反应完毕,该装置中电解质溶液的碱性增强
D.人体呼出的气体参与X电极的反应:CO2+2e-+H2O=CO+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
(1)以甲烷为原料制取氢气是工业上常用的制氢方法。已知:
CH4(g)+H2O(g) = CO(g)+3H2(g)ΔH=+206.2 kJ/mol
CH4(g)+CO2(g) = 2CO(g)+2H2(g)ΔH=+247.4 kJ/mol
CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为________________________。
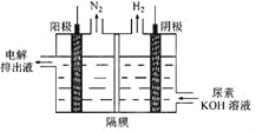
(2)电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图见图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为________________________。
(3) Mg2Cu是一种储氢合金。350℃时,Mg2Cu与H2反应,生成MgCu2和仅含一种金属元素的氢化物(其中氢的质量分数为0.077)。Mg2Cu与H2反应的化学方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有Fe、H2、Ba(OH)2溶液,K2CO3溶液,NaOH溶液,稀硫酸等六种物质,在常温下两种物质间能发生的化学反应最多有
A. 4个 B. 5个 C. 6个 D. 7个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如下图所示,对该反应的推断合理的是( )

A. 该反应的化学方程式为3B+4D![]() 6A+2C
6A+2C
B. 反应进行到1 s时,v(A)=v(D)
C. 反应进行到6 s时,B的平均反应速率为0.05 mol/(L·s)
D. 反应进行到6 s时,各物质的反应速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生为探究钠与二氧化碳的反应,利用如图装置进行实验。

已知PdCl2能被一氧化碳还原得到黑色的Pd。请回答下列问题:
(1)请将上图各装置连接完整:c接f,______接______,______接______,______接______。
(2)若用稀盐酸与碳酸钙反应制备二氧化碳,在加稀盐酸时,发现碳酸钙与稀盐酸不能接触,而稀盐酸又不够了,为使反应能顺利进行,可向长颈漏斗中加入的试剂是______(填字母)。
A.硝酸钠溶液 B.四氯化碳 C.苯 D.稀硝酸
(3)检查装置气密性并装好药品后,点燃酒精灯之前应进行的操作是打开弹簧夹,让二氧化碳充满整个装置,当观察到________________时,再点燃酒精灯。此步操作的目的是________________________________。
(4)反应过程中二氧化碳足量,假如反应过程中有下列两种情况,分别写出两种情况下钠与二氧化碳反应的化学方程式。
Ⅰ.装置⑤PdCl2溶液中观察到有黑色沉淀,装置①中固体成分只有一种,且向固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体: ___________________________。
Ⅱ.装置①中钠的质量为0.46 g,充分反应后,将装置①中的固体加入到足量稀盐酸中产生224 mL(标准状况)二氧化碳气体,且溶液中还有固体残留:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,将这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol·L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
A.60mL B.45mL C.30mL D.无法计算
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com