
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:
在反应X+2Y===R+2M中,已知R和M的摩尔质量之比为22∶9,当1.6 g X与Y完全反应后,生成4.4 g R,则在此反应中Y和M的质量比为( )
A.16∶9
B.23∶9
C.32∶9
D.46∶9
查看答案和解析>>
科目:高中化学 来源: 题型:
发射用的运载火箭使用的是以液氢为燃烧剂,液氧为氧化剂的高能低温推进剂。
已知:H2(g)+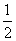 O2(g)===H2O(l)
O2(g)===H2O(l)
ΔH1=-285.8 kJ·mol-1①
H2(g)===H2(l) ΔH2=-0.92 kJ·mol-1②
O2(g)===O2(l) ΔH3=-6.84 kJ·mol-1③
H2O(g)===H2O(l) ΔH4=-44 kJ·mol-1④
下列说法正确的是( )
A.上述四个反应都是吸热反应
B.1 mol液态H2的能量大于1 mol气态H2的能量
C.H2的燃烧热ΔH为-285.8 kJ·mol-1
D.火箭中液氢燃烧的热化学方程式为H2(l)+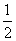 O2(l)===H2O(g) ΔH=-285.8 kJ·mol-1
O2(l)===H2O(g) ΔH=-285.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
某种优质燃油由甲、乙两种有机物混合而成,甲、乙两种物质含有C、H、O三种元素中的两种或三种。已知甲、乙及CO、H2的燃烧热如下:
| 物质 | 甲 | 乙 | CO | H2 |
| 燃烧热/(kJ·mol-1) | 1 366 | 5 518 | 283 | 286 |
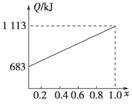
取甲、乙按不同比例混合的燃油23 g,在足量的O2中燃烧时,放出的热量Q与混合物中乙的物质的量分数x的关系如右图所示。试求:
(1)乙的相对分子质量Mr(乙)=________。
(2)160 g由甲、乙以等物质的量混合而成的燃油在347.2 L O2中恰好完全燃烧,得492.8 L气体,冷却到室温时,还剩余224 L(气体体积均在标准状况下测定)。由此可求得混合物中,C、H、O的原子个数比为________。甲、乙的分子式为:甲________;乙________。
(3)1 mol由甲、乙以等物质的量混合而成的燃油在一定量的O2中燃烧,放出热量2 876 kJ,则反应中生成CO________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于“化学之最”, 下列说法正确的是( )
①铝是地壳里含量最多的金属元素②第六周期是目前周期表中含元素最多的周期
③Na是短周期元素中原子半径最大的主族元素 ④F是非金属最强的元素
A.全对 B.除①外全对 C.除②外全对 D.除③外全对
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
| 周期 族 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)金属性最强的是 _,化学性质最不活泼的是__________。
(2)②、③、⑨的最高价含氧酸的酸性由强到弱的顺序是_____________。(填化学式)
(3)⑧的原子结构示意图为_________________,硒(Se)是人体必需的微量元素,与⑧同一主族且比⑧原子多一个电子层,则Se的原子序数为___________。
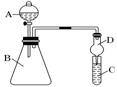 (4)若要证明非金属性:⑨>碘, 可向A中加浓盐酸,B中加KMnO4,(常温下KMnO4与浓盐酸反应),C中加淀粉碘化钾混合溶液,观察到C溶液中现象为___________,即可证明。
(4)若要证明非金属性:⑨>碘, 可向A中加浓盐酸,B中加KMnO4,(常温下KMnO4与浓盐酸反应),C中加淀粉碘化钾混合溶液,观察到C溶液中现象为___________,即可证明。
查看答案和解析>>
科目:高中化学 来源: 题型:
COCl2(g) CO(g)+Cl2(g) ΔH>0。当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
CO(g)+Cl2(g) ΔH>0。当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
A.①②④ B.①④⑥
C.②③⑤ D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关甲苯的实验事实中,能说明侧链对苯环性质有影响的是 ( )
A.甲苯的硝化反应生成三硝基甲苯 B.甲苯能使酸性高锰酸钾溶液褪色
C.甲苯燃烧产生带浓烟的火焰 D.1mol甲苯与3mol H2发生加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com